Bohr Modeli |
|
|
#1 |
|
Şengül Şirin

|
Bohr ModeliBohr modeli Bu Bohr Teorisi ve Balmer-Rydberg Denklemi Bu yazı veya bölüm halinde birleştirilmiş önerdi olmuştur  ( Discuss ) (Tartışma)   ) The Rutherford-hidrojen atomu ve Bohr modeli (Z = 1) veya iyon gibi bir hidrojen (Z> 1), burada olumsuz ücret elektron bir atom kabuk yapılan küçük bir olumlu ücret atom çekirdeği encircles, yörünge arasında bir elektron atlamak eşliğinde bir emitted veya elektromanyetik enerji (hν) miktarı emilir      Atom fizik olarak, Bohr modeli Niels Bohr tarafından oluşturulan bir küçük olumlu ücret çekirdek elektronlar tarafından çevrili olarak atomu gösteriyor bu çekirdek etrafında dairesel yörünge yolculuk-yapısı bir güneş sistemi gibi, ama elektrostatik kuvvetlerin çekilmesi sağlayarak yerine ile yerçekimi  Bu, daha önce kübik modeli (1902) bir gelişme olduğunu, bu erik-puding modeli (1904), ve Satürn modeli (1904) ve Rutherford modeli (1911) Bu, daha önce kübik modeli (1902) bir gelişme olduğunu, bu erik-puding modeli (1904), ve Satürn modeli (1904) ve Rutherford modeli (1911) Rutherford-Bohr model Çünkü Bohr modeli kuantum fiziği söyledi-Rutherford modeli değişiklik tabanlı, çok kaynak, bu Rutherford-Bohr modeline atıfta iki birleştirir    model was introduced While the Rydberg formül deneysel bilinen olduğunu, bir teorik kadar Bohr modeli tanıtılan underpinning elde değildi  Sadece Bohr modeli Rydberg formülün yapısını sebebini açıklayabilir ama bu temel fiziksel sabitlerin açısından kendi deneysel sonuçlar için bir mazeret sağladı Sadece Bohr modeli Rydberg formülün yapısını sebebini açıklayabilir ama bu temel fiziksel sabitlerin açısından kendi deneysel sonuçlar için bir mazeret sağladı Bir teori olarak, hidrojen atomu bir ilk sırada yaklaşık olarak kuantum mekaniği ve çok daha doğru geniş kullanarak ve türemek böylelikle eski bir bilimsel teori olarak kabul edilebilir      (1900) ve bir tam gelişmiş kuantum mekaniği (1925) ve Advent ve Planck's keşif arasındaki dönemde ve kuantum kuramı genellikle için eski kuantum teorisi olarak anılır (1900) ve bir tam gelişmiş kuantum mekaniği (1925) ve Advent ve Planck's keşif arasındaki dönemde ve kuantum kuramı genellikle için eski kuantum teorisi olarak anılır Origin s Erken 20  yüzyılda, Ernest Rutherford tarafından deneyler bu atomları olumsuz ücret elektronlar küçük, yoğun çevre, olumlu çekirdek ücret bir diffuz bulut oluşuyordu kurdu yüzyılda, Ernest Rutherford tarafından deneyler bu atomları olumsuz ücret elektronlar küçük, yoğun çevre, olumlu çekirdek ücret bir diffuz bulut oluşuyordu kurdu Bu deneysel veriler göz önüne alındığında, Rutherford doğal olarak, 1911 ve Rutherford modeli - elektron bir güneş çekirdeği yörüngede - Ancak gezegen söyledi modeli atomu bir teknik zorluk bir gezegen model atomu olarak Bu deneysel veriler göz önüne alındığında, Rutherford doğal olarak, 1911 ve Rutherford modeli - elektron bir güneş çekirdeği yörüngede - Ancak gezegen söyledi modeli atomu bir teknik zorluk bir gezegen model atomu olarak nucleus Klasik mekanik bir yasa (), bir çekirdek yörüngede olan elektron elektromanyetik radyasyon yayımı önceden bu LARMOR formül yani  Çünkü elektron, bu da yavaş yavaş helezon içe doğru olan çekirdek içine çöken enerji kaybedecek Çünkü elektron, bu da yavaş yavaş helezon içe doğru olan çekirdek içine çöken enerji kaybedecek model is Çünkü tüm atomları kararsız olduğunu tahmin Bu atomu modeli, bir felaket Ayrıca, elektron Sarmallar içlerine, bir emisyon kademeli frekans artışı da olarak yörüngesi var küçük ve hızlı    Ancak, tahliye cam tüpler çeşitli düşük basınç gasses ile elektrik deşarj ile geç 19 Ancak, tahliye cam tüpler çeşitli düşük basınç gasses ile elektrik deşarj ile geç 19 yüzyılda deneyler bu atomları sadece yayınlamaz ışık sağlayacak vardı (bazı ayrık frekanslarda, elektromanyetik radyasyon) olduğunu yüzyılda deneyler bu atomları sadece yayınlamaz ışık sağlayacak vardı (bazı ayrık frekanslarda, elektromanyetik radyasyon) olduğunu   : O önerilen bu elektron olabilir sadece belirli klasik hareketleri:
 Çünkü emisyon süreci iki farklı dönemlerde iki yörünge içerir rağmen kural 3 tamamen iyi küçük yörünge için tanımlı değilse, Bohr sınırlı enerji düzeyleri kural 3 kullanan ve tam olarak doğru kuantum kural gelmek arasındaki aralığı: bu açısal momentum L belirlemek olabilir sabit bir birimin bir tamsayı birden fazla değer: Çünkü emisyon süreci iki farklı dönemlerde iki yörünge içerir rağmen kural 3 tamamen iyi küçük yörünge için tanımlı değilse, Bohr sınırlı enerji düzeyleri kural 3 kullanan ve tam olarak doğru kuantum kural gelmek arasındaki aralığı: bu açısal momentum L belirlemek olabilir sabit bir birimin bir tamsayı birden fazla değer:  where n = 1, 2, 3, burada n = 1, 2, 3,       is called the principal quantum number , and ħ = h /2π temel kuantum numarası ve H = S denir / 2π  The lowest value of n is 1; this gives a smallest possible orbital radius of 0 N en düşük değeri 1 ise, bu 0,0529 mil olan Bohr yarıçapı olarak bilinen bir küçük olası yörünge yarıçapı sağlar 0529 nm known as the Bohr radius 0529 nm known as the Bohr radius   Once an electron is in this lowest orbit, it can get no closer to the proton Bir elektron bu düşük yörüngeye in, it is no yakın Proton için alabilirsiniz  Starting from the angular momentum quantum rule Bohr [ 1 ] was able to calculate the energies of the allowed orbits of the hydrogen atom and other hydrogen-like atoms and ions Ve açısal momentum kuantum kural kimden Bohr Başlangıç [1] hidrojen atomu ve diğer hidrojen izin verilen yörünge ve enerji-atom ve iyonları gibi hesaplamak mümkün oldu  Other points are: Diğer noktalar:
__________________
Arkadaşlar, efendiler ve ey millet, iyi biliniz ki, Türkiye Cumhuriyeti şeyhler, dervişler, müritler, meczuplar memleketi olamaz
 En doğru, en hakiki tarikat, medeniyet tarikatıdır En doğru, en hakiki tarikat, medeniyet tarikatıdır |

|
Cevap : Bohr Modeli |
|
|
#2 |
|
Şengül Şirin

|
Cevap : Bohr Modeli: Bohr koşulunun, bu açısal momentum H tamsayı çok sonra De Broglie bir duran dalga şartı olarak reinterpreted was: elektron bir dalga ve wavelengths bir tam sayı ile elektron's yörüngeye bir çember boyunca sığmalıdır açıklanmıştır:  Substituting de Broglie's wavelength reproduces Bohr's rule Yerine De Broglie's dalga Bohr iktidarı üretir  Bohr ve yazışmaların ilkesine çekici tarafından bir dalga yorumu veren olmaksızın kendi kural haklı Bohr ve yazışmaların ilkesine çekici tarafından bir dalga yorumu veren olmaksızın kendi kural haklı 1925 yılında mekanik yeni bir tür, in which elektron quantized yörünge içinde seyahat ve Bohr model elektron hareket daha doğru bir modeli olarak genişletilmiş oldu kuantum mekaniği önerilmişti  Yeni teori Werner Heisenberg tarafından önerilmişti Yeni teori Werner Heisenberg tarafından önerilmişti Için aynı teori başka bir formu, modern kuantum mekaniği, Avusturyalı fizikçi Erwin Schrödinger tarafından bağımsız olarak keşfetti ve farklı bir mantık ile Için aynı teori başka bir formu, modern kuantum mekaniği, Avusturyalı fizikçi Erwin Schrödinger tarafından bağımsız olarak keşfetti ve farklı bir mantık ile elektron enerji düzeyleri The Bohr modeli sistemi için hemen hemen kesin sonuç verir nerede hızları çok daha az iki ücret puanı yörüngede birbirlerine ışık bu  Bu sadece bir elektron sistemleri, hidrojen atomu gibi tek başına-ionized helyum, iki kat lityum ionized içerir, ama burada bir elektron uzak herşey kimden olduğunu positronium ve Atom Rydberg devletler içerir Bu sadece bir elektron sistemleri, hidrojen atomu gibi tek başına-ionized helyum, iki kat lityum ionized içerir, ama burada bir elektron uzak herşey kimden olduğunu positronium ve Atom Rydberg devletler içerir Bu for K-hat X-ray geçiş hesaplamalar diğer varsayımlar eklenir (aşağıda) Moseley yasası görmek kullanılabilir Bu for K-hat X-ray geçiş hesaplamalar diğer varsayımlar eklenir (aşağıda) Moseley yasası görmek kullanılabilir   : Bir yörünge hesaplamak için iki varsayımlar gerektirir: 1  Klasik mekanik Klasik mekanik        radius: Bu herhangi bir yarıçapı hızını belirler:  Ayrıca herhangi bir yarıçapı toplam enerji belirler: Ayrıca herhangi bir yarıçapı toplam enerji belirler:  Toplam enerji ve R ters orantılı olumsuz Toplam enerji ve R ters orantılı olumsuz   sonsuz değerleri için, enerji sıfır, hareketsiz bir elektron karşılık gelen sonsuz kadar Proton değil sonsuz değerleri için, enerji sıfır, hareketsiz bir elektron karşılık gelen sonsuz kadar Proton değil the Toplam enerji hangi olmayan dairesel yörünge için de geçerlidir yarısı potansiyel enerji, bu virial teoremi de gereğidir  For larger nuclei, the only change is that k e e 2 is everywhere replaced by Zk e e 2 where Z is the number of protons Büyük nükleuslar için, tek değişiklik nerede Z protons sayısı o K e E 2 her ZK e E 2 yerini olmasıdır  For positronium , m e is replaced by its reduced mass ( μ = m e /2 ) Positronium için, M ve E düşmüş kitle tarafından (μ = m E / 2) ile değiştirilir  2 2 Kuantum kural Kuantum kural : Bu açısal momentum L = m E VR H tamsayı birden fazla ise: 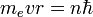 Hız için ifadesi yerine n açısından R bir denklemi verir: Hız için ifadesi yerine n açısından R bir denklemi verir:  böylelikle herhangi n izin verilen yörüngeye yarıçaptır: böylelikle herhangi n izin verilen yörüngeye yarıçaptır:  R en küçük olası değeri Bohr denilen bir yarıçap ve eşittir: R en küçük olası değeri Bohr denilen bir yarıçap ve eşittir: 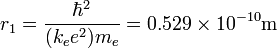 N ve enerji inci düzeyi yarıçapı ile belirlenir: N ve enerji inci düzeyi yarıçapı ile belirlenir: 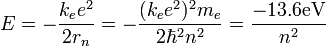     ( R E ): Enerji formülü doğal sabitlerin bir kombinasyonu Rydberg enerji (R E) denir:  : Bu ifade daha fazla doğal birimleri formu kombinasyonları olarak yorumlama ile açıklanabilir:  is the rest mass energy of the electron (511 keV/c) elektron (511 Kev / c) geri kalan kitle enerjidir  is the fine structure constant ve ince yapısı sabit bir    Bu Şimdi bulunduğu bir kaba sipariş gerçek enerji seviyelerinin büyüklüğü yaklaşık olarak hizmet verebilir Yani, Z protons ile nükleuslar için, enerji seviyelerini bir kaba tahminler () için: Bu Şimdi bulunduğu bir kaba sipariş gerçek enerji seviyelerinin büyüklüğü yaklaşık olarak hizmet verebilir Yani, Z protons ile nükleuslar için, enerji seviyelerini bir kaba tahminler () için: 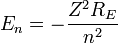     Ne zaman Z = 1 / α (Z ≈ 137), hareket yüksek, relativistic olur ve Z 2 R ve α 2 iptal olan yörüngede enerji enerji geri kalan karşılaştırılabilir olmaya başlar  Yeterince büyük esaslar, eğer istikrarlı ise, vakum bir bağlı elektron oluşturarak, sonsuza için pozitif çkardktan kendi şarj azaltmak olacaktır Yeterince büyük esaslar, eğer istikrarlı ise, vakum bir bağlı elektron oluşturarak, sonsuza için pozitif çkardktan kendi şarj azaltmak olacaktır Bu maksimum nükleer ücreti öngörür elektromanyetik şarj tarama teorik olgudur Bu maksimum nükleer ücreti öngörür elektromanyetik şarj tarama teorik olgudur  [ citation needed ] [ citation needed ] Positronium için, formülü azaltılmış kitle kullanır  Yarıçapı, elektron ve pozitif bir değer için her toplu ortak merkez etrafında at yarısı hızlı hareket ediyor ve her bir tek dördüncü bir kinetik enerji vardır Yarıçapı, elektron ve pozitif bir değer için her toplu ortak merkez etrafında at yarısı hızlı hareket ediyor ve her bir tek dördüncü bir kinetik enerji vardır Toplam kinetik enerji yarısı tek bir elektron ağır bir çekirdek etrafında hareket için ne olur Toplam kinetik enerji yarısı tek bir elektron ağır bir çekirdek etrafında hareket için ne olur  (positronium) (positronium) Rydberg formülü   Bohr's formül ve sayısal değerini verir zaten bilinen ve ölçülen Rydberg's ama şimdi elektron's ücret ve Planck's sabit dahil doğanın daha temel sabitlerin of açısından sürekli Bohr's formül ve sayısal değerini verir zaten bilinen ve ölçülen Rydberg's ama şimdi elektron's ücret ve Planck's sabit dahil doğanın daha temel sabitlerin of açısından sürekli Ne zaman başka bir enerji düzeyine gelen elektron hamle, bir foton emitted olduğunu   Bir foton bir hidrojen atomu ile emitted ve enerji iki hidrojen enerji seviyelerinin fark verilir: 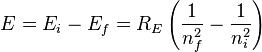   Since the energy of a photon is Bir ışık ve enerji bu yana ise  the wavelength of the photon given off is given by the foton dışı verilen bir dalga boyu ile    Bu formül ondokuzuncu yüzyılda bilim spektroskopi çalışmaları için, ama bilinen olduğunu orada Bohr kadar bu formu veya R değeri için teorik bir öngörü, hiçbir teorik açıklama Gerçekte, Rydberg sabit ve Bohr's türetme yanı sıra Lyman (n f = 1), Balmer (n F = 2) deneysel gözlenen spektral çizgileri ile Bohr's formülün ve beraberindeki anlaşma ve Paschen (n f = 3) dizi ve diğer satırlar henüz gözlenen değil başarılı kuramsal tahmini, bir nedeni onun modeli hemen kabul edildi Bu formül ondokuzuncu yüzyılda bilim spektroskopi çalışmaları için, ama bilinen olduğunu orada Bohr kadar bu formu veya R değeri için teorik bir öngörü, hiçbir teorik açıklama Gerçekte, Rydberg sabit ve Bohr's türetme yanı sıra Lyman (n f = 1), Balmer (n F = 2) deneysel gözlenen spektral çizgileri ile Bohr's formülün ve beraberindeki anlaşma ve Paschen (n f = 3) dizi ve diğer satırlar henüz gözlenen değil başarılı kuramsal tahmini, bir nedeni onun modeli hemen kabul edildi Atom Kabuk modeli Bohr ağır atomları için yaklaşık modeli vermek Hidrojen örnek verdi        Sonra yörüngeye tam, sonraki düzey kullanılan gerekiyor Sonra yörüngeye tam, sonraki düzey kullanılan gerekiyor   Çünkü olmayan her kabuk bir elektron-etkileşime davranır Bu model daha hidrojen model daha yaklaşıktır  But the repulsions of electrons is taken into account somewhat by the phenomenon of screening Ama elektron ve repulsions dikkate biraz tarama bir olgu tarafından alınır    Örneğin, lityum atomu en düşük 1S yörüngede ve bu yörüngede iki elektron vardır Z = 2  Her bir tarama etkisi Z = 3 eksi bir nükleer şarj gördüğü, başka hangi crudely nükleer ücret azaltır 1 birim tarafından Her bir tarama etkisi Z = 3 eksi bir nükleer şarj gördüğü, başka hangi crudely nükleer ücret azaltır 1 birim tarafından Bu da yaklaşık 1/4th ve Bohr yarıçapı en içteki elektron yörünge Bu da yaklaşık 1/4th ve Bohr yarıçapı en içteki elektron yörünge 2 At lityum yörünge en dıştaki elektron kabaca Z = 1, iki iç elektronlar 2 ile nükleer ücret azaltmak beri  Bu dış elektron olan çekirdek yaklaşık bir Bohr yarıçapı olmalıdır Bu dış elektron olan çekirdek yaklaşık bir Bohr yarıçapı olmalıdır Çünkü elektronlar güçlü birbirlerini itme, etkin şarj açıklamasına çok Z genellikle çıkmak değildir etkin şarj tamsayı olarak yaklaşıktır Çünkü elektronlar güçlü birbirlerini itme, etkin şarj açıklamasına çok Z genellikle çıkmak değildir etkin şarj tamsayı olarak yaklaşıktır , Ama Moseley yasası deneysel probları elektron ve içteki Pair, ve bu dıştaki kabuk sadece bir elektron bir atomu veya iyon en dıştaki elektron etkili şarj ZK ile temel yörünge bunların yaklaşık Z nükleer şarj-1 görüyorum gösterir burada K iç kabuk olarak elektron toplam sayıdır   yüzyılda codified oldu atomları en gizemli özelliklerinin çok açıklamak mümkün oldu yüzyılda codified oldu atomları en gizemli özelliklerinin çok açıklamak mümkün oldu Bir mülkiyet atomları olan kararlı olabilir boyutu yaklaşık gazlar ve saf kristal katı bir yoğunluk ve viskozite ölçüm yaptı Bir mülkiyet atomları olan kararlı olabilir boyutu yaklaşık gazlar ve saf kristal katı bir yoğunluk ve viskozite ölçüm yaptı   Tablonun sağ Atomlar süre sola atomları onları kaybetmek eğilimindedir, elektron elde eğilimindedir Tablonun sağ Atomlar süre sola atomları onları kaybetmek eğilimindedir, elektron elde eğilimindedir   Kabuk modeli, bu olgu kabuk tarafından açıklanmıştır-doldurma  Müteakip atomları kadar yörüngeye, bu tablonun bir sonraki atomu noktası dolu çünkü, aynı boyuttaki yörünge doldurma bir gevşek bağlı dış elektron vardır küçük genişletin neden alıyorum Müteakip atomları kadar yörüngeye, bu tablonun bir sonraki atomu noktası dolu çünkü, aynı boyuttaki yörünge doldurma bir gevşek bağlı dış elektron vardır küçük genişletin neden alıyorum   Ikinci yörüngeye, ve bu atomu dolu sekiz elektron sağlar neon, daha hareketsiz olduğu Ikinci yörüngeye, ve bu atomu dolu sekiz elektron sağlar neon, daha hareketsiz olduğu Üçüncü yörünge daha, daha doğru Sommerfeld tedavi dışında sekiz içerir (modern kuantum mekaniği olarak) bu "ekstra d" elektron vardır çoğaltılamaz Üçüncü yörünge daha, daha doğru Sommerfeld tedavi dışında sekiz içerir (modern kuantum mekaniği olarak) bu "ekstra d" elektron vardır çoğaltılamaz   Bu düzensiz dolgu deseni elektronlar arasında da dikkate ya Bohr veya Sommerfeld modelleri, ve hatta modern tedavisinde hesaplamak zor alınan değildir etkileşimler, bir etkisidir Bu düzensiz dolgu deseni elektronlar arasında da dikkate ya Bohr veya Sommerfeld modelleri, ve hatta modern tedavisinde hesaplamak zor alınan değildir etkileşimler, bir etkisidir Moseley yasası ve K hesaplama-alfa X ışını emisyon çizgileri " Niels Bohr 1962 dedi, "Sen gerçekten Rutherford eser [nükleer atomu görmek] ciddiye alınan değildi Bugün anlamıyoruz, ancak tüm ciddiye alınan değildi Bugün anlamıyoruz, ancak tüm ciddiye alınan değildi Bunun hiçbir söz herhangi bir yerdi Bunun hiçbir söz herhangi bir yerdi Büyük değişiklik geldi Moseley den Büyük değişiklik geldi Moseley den " " 1913 Henry Moseley olarak (sonra K olarak bilinen-alfa hattı), ve en güçlü X-ray hattı elektron bombardıman altında atomları tarafından emitted arasında ampirik bir ilişki bulunan ve atom numarası Z  Moseley s' şarlatan formülü Rydberg ve Bohr's türetilebilir olduğu formül (Moseley aslında modeller açısından) sadece Ernest Rutherford ve Antonius Van den Broek sözetmektedir Moseley s' şarlatan formülü Rydberg ve Bohr's türetilebilir olduğu formül (Moseley aslında modeller açısından) sadece Ernest Rutherford ve Antonius Van den Broek sözetmektedir Bu, X-ray hattı kuantum numaraları 1 ve 2 ile enerji düzeyleri arasında bir geçiş, ve geldi [2], bu Z zaman hidrojen atomları daha ağır için formül olarak kullanılan atom numarası olmalıdır 1, azaltılmış için (Z-1) ² Bu, X-ray hattı kuantum numaraları 1 ve 2 ile enerji düzeyleri arasında bir geçiş, ve geldi [2], bu Z zaman hidrojen atomları daha ağır için formül olarak kullanılan atom numarası olmalıdır 1, azaltılmış için (Z-1) ² Moseley Bohr için, onun sonuçları hakkında şaşkın yazdım, ama Bohr yardım edemedi      Daha sonra, insanlar etkisini şarj taraması ile, bir iç kabuğu 2 elektron içeren neden anlaşıldı  Deneme olarak, bir atomu en içteki elektron, bir tek kalan elektron içeren düşük Bohr yörüngesi, bir boşluğa bırakarak dışarı knocked olduğunu Deneme olarak, bir atomu en içteki elektron, bir tek kalan elektron içeren düşük Bohr yörüngesi, bir boşluğa bırakarak dışarı knocked olduğunu n=2 Bu pozisyon sonra = 2 n sahip bir sonraki yörüngede, bir elektron tarafından doldurulur  Ama n = 2 elektron Z etkili bir şarj-1 olan değerini tek bir elektron en düşük Bohr yörüngede nükleer ücret + Z ekrana kalan çekirdek, ve şarj için uygun olup olmadığını görmek ve bu alt -- 1 (elektron negatif şarj nükleer olumlu ücret tarama) dolayı Ama n = 2 elektron Z etkili bir şarj-1 olan değerini tek bir elektron en düşük Bohr yörüngede nükleer ücret + Z ekrana kalan çekirdek, ve şarj için uygun olup olmadığını görmek ve bu alt -- 1 (elektron negatif şarj nükleer olumlu ücret tarama) dolayı Enerji bir elektron ikinci shell ilk için atılan bulunarak elde for K Moseley yasası-alfa satırları verir: Enerji bir elektron ikinci shell ilk için atılan bulunarak elde for K Moseley yasası-alfa satırları verir:  or veya  sabit Burada, R v = R E / h ise, frekans 3,28 eşit açısından x 10 15 Hz sabit Burada, R v = R E / h ise, frekans 3,28 eşit açısından x 10 15 Hzby 0 11 ve 31 Bu son ilişki arasında Z değerleri için empirically Moseley tarafından, basit bir (dikey olarak) X kare kök arsa-atom numarası ışını frekansı elde olmuştur (ancak, gümüş için, Z = 47, ve deneysel elde tarama terim 0,4 ile) değiştirilmelidir 4) 4)    satır şimdi kapatılacak satırlar bir çift, (K α1 ve K α2) Siegbahn notasyon olarak yazılı olarak bilinir  eksiklikleri The Bohr modeli yanlış bir değer verir 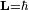 for the ground state orbital angular momentum zemin devlet yörünge açısal momentum için  Gerçek zemin devlet içindeki açısal momentum sıfır olarak bilinir Gerçek zemin devlet içindeki açısal momentum sıfır olarak bilinir Her ne kadar akıl fotoğraf biraz ölçekli, hayır yörünge ivme ile en düşük modern "yörünge bir elektron" bu düzeyde, başarısız "" olan çekirdek tüm etrafında döndürmek olarak değil, ama olabilir sadece sıkıca çevresinde bir gitmek sıfır alanı elips (bu "geri" olarak, çarpıcı veya çekirdek ile etkileşim olmadan) resim olabilir Her ne kadar akıl fotoğraf biraz ölçekli, hayır yörünge ivme ile en düşük modern "yörünge bir elektron" bu düzeyde, başarısız "" olan çekirdek tüm etrafında döndürmek olarak değil, ama olabilir sadece sıkıca çevresinde bir gitmek sıfır alanı elips (bu "geri" olarak, çarpıcı veya çekirdek ile etkileşim olmadan) resim olabilir   Yine de, hatta en karmaşık semiclassical modeli de en düşük enerji durumu spherically simetrik olduğunu --- bu yönde herhangi bir bağlantısı yoktur açıklamak için başarısız olur Yine de, hatta en karmaşık semiclassical modeli de en düşük enerji durumu spherically simetrik olduğunu --- bu yönde herhangi bir bağlantısı yoktur açıklamak için başarısız olur Modern kuantum mekaniği olarak, hidrojen ve elektron olasılık olan çekirdek yakınlarında yoğun büyüyen bir küresel bulut olduğunu  " Bu oran-Olasılık sabit-hidrojen olarak çürümesi ve Bohr yarıçapı ters, ama eşittir beri Bohr dairesel yörünge değil, sıfır alan elipsler, bu iki sayının tam olarak bu gerçeği kabul ile çalıştı, bir tesadüf olarak kabul ediliyor modern quantum mechanics) (Her ne kadar çok bu tür tesadüfi anlaşmalar yarı arasında bulunan vs the Atom tam kuantum mekanik tedavi klasik; bu hidrojen atomu özdeş enerji düzeyleri vardır ve bu relativistic Bohr kimden doğar ince yapısı sabit, bir türevini-Sommerfield Model (aşağıya bakınız), ve tamamen farklı bir konsept ile eşit olması için, tam çağdaş kuantum mekaniği olur)  The Bohr modeli de, ya da zorluk vardır başka açıklamaya başarısız:
Ayrıntılandırmalar It has been suggested that this article or section be merged with Bohr–Sommerfeld theory Bu makale veya bölüm Bohr ile birleştirilmiş olmak Sommerfeld kuramı önerdi olmuştur  ( Discuss ) (Tartışma)  Eliptik aynı enerji ve quantized açısal momentum ile yörünge   Burada P r radyal hız canonically olan Q olan radyal konum ve T koordine etmek birleşik bir tam yörünge süresi Burada P r radyal hız canonically olan Q olan radyal konum ve T koordine etmek birleşik bir tam yörünge süresi ntegre eylem eylem açı olduğunu koordinatları ntegre eylem eylem açı olduğunu koordinatları       Bu açık gerçek bir atomu bu şekilde açılır ve bu kısıtlama olmadan koordinatları göre contradicted Bu açık gerçek bir atomu bu şekilde açılır ve bu kısıtlama olmadan koordinatları göre contradicted Bu Sommerfeld nicemleme farklı kanonik koordinatlarıdır ve yapılabilir bazen hangi farklı cevaplar verir Bu Sommerfeld nicemleme farklı kanonik koordinatlarıdır ve yapılabilir bazen hangi farklı cevaplar verir radiation/atom system, which is difficult when the radiation is allowed to escape Çünkü bu hareket bulunması gereken açı radyasyon düzeltme ve Incorporation zor bir kombine radyasyon için koordine eden bir radyasyon kaçmak için izin verilir zordur atomu sistemi   atom , Sonunda, model, modern kuantum tarafından ilk Wolfgang Pauli tarafından 1925 yılında verilmiş olan hidrojen atomu, Heisenberg "matris mekaniği lar kullanarak mekanik tedavi değiştirildi  T Hidrojen atomu en güncel resmi Erwin Schrödinger 1926 yılında geliştirilen dalga mekaniği ve atomik yörüngeler dayanmaktadır Ancak, bu sorunun Bohr modeli onun başarıları ile olduğu anlamına gelmez        Bu fark arkasındaki yaygın teori olan elektron ve enerji durumuna göre değişir elektronlar, en yörüngeler ve şekiller yatıyor Bu fark arkasındaki yaygın teori olan elektron ve enerji durumuna göre değişir elektronlar, en yörüngeler ve şekiller yatıyor The Bohr-Sommerfeld nicemleme koşulları, modern matematik alanında sorulara yol açmaktadır  Tutarlı semiclassical nicemleme koşulu faz space yapısı hangi quantized olabilir symplectic manifolds türleri üzerinde topolojik sınırlamalar yerlerde belirli bir türünü gerektirir Tutarlı semiclassical nicemleme koşulu faz space yapısı hangi quantized olabilir symplectic manifolds türleri üzerinde topolojik sınırlamalar yerlerde belirli bir türünü gerektirir 
__________________
Arkadaşlar, efendiler ve ey millet, iyi biliniz ki, Türkiye Cumhuriyeti şeyhler, dervişler, müritler, meczuplar memleketi olamaz
 En doğru, en hakiki tarikat, medeniyet tarikatıdır En doğru, en hakiki tarikat, medeniyet tarikatıdır |

|
Üye olmanıza kesinlikle gerek yok !
Konuya yorum yazmak için sadece buraya tıklayınız.
Bu sitede 1 günde 10.000 kişiye sesinizi duyurma fırsatınız var.
IP adresleri kayıt altında tutulmaktadır. Aşağılama, hakaret, küfür vb. kötü içerikli mesaj yazan şahıslar IP adreslerinden tespit edilerek haklarında suç duyurusunda bulunulabilir.
Konuya yorum yazmak için sadece buraya tıklayınız.
Bu sitede 1 günde 10.000 kişiye sesinizi duyurma fırsatınız var.
IP adresleri kayıt altında tutulmaktadır. Aşağılama, hakaret, küfür vb. kötü içerikli mesaj yazan şahıslar IP adreslerinden tespit edilerek haklarında suç duyurusunda bulunulabilir.
«
Önceki Konu
|
Sonraki Konu
»
|
|
ForumSinsi.com hakkında yapılacak tüm şikayetlerde ilgili adresimizle iletişime geçilmesi halinde kanunlar ve yönetmelikler çerçevesinde en geç 1 (Bir) Hafta içerisinde gereken işlemler yapılacaktır. İletişime geçmek için buraya tıklayınız.







