Biyokimya (1.BÖLÜM) |
|
|
#1 |
|
Şengül Şirin

|
Biyokimya (1.BÖLÜM)Biyokimya, adından da anlaşılacağı gibi canlı organizmalar ve bu organizmaları meydana getiren hücrelerde meydana gelen metabolik faaliyetleri inceleyen bilim dalıdır  Aynı zamanda biyokimya, moleküler biyoloji ile sıkı bir ilişki içerisindedir  Biyokimya konusunda esas olarak canlı hücrelerinde cereyan eden kimyasal tepkime basamaklarını, bu basamaklara etki eden katalizör görevindeki enzimleri, fotosentezi ve solunum konusunu ele almaya çalışacağız Biyokimya konusunda esas olarak canlı hücrelerinde cereyan eden kimyasal tepkime basamaklarını, bu basamaklara etki eden katalizör görevindeki enzimleri, fotosentezi ve solunum konusunu ele almaya çalışacağız Bu konular haricinde biyokimya bilim dalının incelediği sayısız metabolik reaksiyon vardır Bu konular haricinde biyokimya bilim dalının incelediği sayısız metabolik reaksiyon vardır Örneğin karbonhidrat metabolizması, fotosentezin izlediği alternatif yollar, yağların yıkımı, proteinlerin yıkımı gibi Örneğin karbonhidrat metabolizması, fotosentezin izlediği alternatif yollar, yağların yıkımı, proteinlerin yıkımı gibi Sayfamızda bu metabolik olayları özetleyerek tek tek ele alacağız Sayfamızda bu metabolik olayları özetleyerek tek tek ele alacağız Amino Asitler Canlı organizmaların temelini nasıl hücreler meydana getiriyor ise, hücrelerin temelinide proteinler meydana getirir  Protein molekülleri hücreyi inşaa eden birer tuğla gibidir Protein molekülleri hücreyi inşaa eden birer tuğla gibidir Amino asitler ise proteinleri meydana getiren daha küçük moleküllerdir Amino asitler ise proteinleri meydana getiren daha küçük moleküllerdir Yani amino asitler uzun zincirler oluşturarak proteinleri, proteinlerde kompleks bir şekilde organize olarak hücreyi meydana getirir Yani amino asitler uzun zincirler oluşturarak proteinleri, proteinlerde kompleks bir şekilde organize olarak hücreyi meydana getirir Tabii karmaşık bir yapıya sahip olan hücre yanlızca proteinlerden oluşmaz  Bunun yanında karbonhidratlar, yağlar, glikolipidler, fosfolipidler ve DNA - RNA molekülleri gibi kimysal maddelerde hücrenin yapısına katılırlar Bunun yanında karbonhidratlar, yağlar, glikolipidler, fosfolipidler ve DNA - RNA molekülleri gibi kimysal maddelerde hücrenin yapısına katılırlar Fakat proteinsiz bir hücre düşünmek mümkün değildir Fakat proteinsiz bir hücre düşünmek mümkün değildir İlk olarak proteinleri meydana getiren en ufak birim olan amino asitlerin kimyasal yapılarını ve diğer özelliklerini tablo halinde ele alalım  No : Amino asit Kimyasal formülü M  A A (gr/mol) İzoelektrik nok (gr/mol) İzoelektrik nok Sembolü 1-) Alanin C3-H7-N-02 89 6,0 Ala 2-) Arjinin C6-H14-N4-O2 174 11,15 Arg 3-) Asparagin C4-H8-N2-O 132 5,41 Asn 4-) Aspartik asit C4-H7-N-04 133 2,77 Asp 5-) Fenil alanin C9-H6-N-O2 ~ 165 5,48 Phe 6-) Glutamin C5-H10-N2-O3 146 5,65 Gln 7-) Glutamik asit C5-H9-N-O4 147 3,22 Glu 8-) Glisin C2-H5-N-O2 75 5,97 Gly 9-) Histidin C6-H8-N3-O2 144 7,47 His 10-) İzolösin C6-H13-N-O2 131 5,94 İle 11-) Lösin C6-H13-N-O2 131 5,98 Leu 12-) Lizin C6-H14-N2-O2 146 9,59 Lys 13-) Metionin C5-H11-N-O2-S 149 5,74 Met 14-) Prolin C5-H9-N-O2 115 6,3 Pro 15-) Serin C3-H7-N-O2 105 5,68 Ser 16-) Sistein C3-H7-N-O2-S 121 5,02 Cys 17-) Treonin C4-H9-N-O3 119 5,64 Thr 18-) Triptofan C11-H8-N2-O2 ~ 204 5,89 Trp 19-) Tirozin C9-H7-N-O3 ~ 181 5,66 Tyr 20-) Valin C5-H11-N-O2 117 5,96 Val Sembolü 1-) Alanin C3-H7-N-02 89 6,0 Ala 2-) Arjinin C6-H14-N4-O2 174 11,15 Arg 3-) Asparagin C4-H8-N2-O 132 5,41 Asn 4-) Aspartik asit C4-H7-N-04 133 2,77 Asp 5-) Fenil alanin C9-H6-N-O2 ~ 165 5,48 Phe 6-) Glutamin C5-H10-N2-O3 146 5,65 Gln 7-) Glutamik asit C5-H9-N-O4 147 3,22 Glu 8-) Glisin C2-H5-N-O2 75 5,97 Gly 9-) Histidin C6-H8-N3-O2 144 7,47 His 10-) İzolösin C6-H13-N-O2 131 5,94 İle 11-) Lösin C6-H13-N-O2 131 5,98 Leu 12-) Lizin C6-H14-N2-O2 146 9,59 Lys 13-) Metionin C5-H11-N-O2-S 149 5,74 Met 14-) Prolin C5-H9-N-O2 115 6,3 Pro 15-) Serin C3-H7-N-O2 105 5,68 Ser 16-) Sistein C3-H7-N-O2-S 121 5,02 Cys 17-) Treonin C4-H9-N-O3 119 5,64 Thr 18-) Triptofan C11-H8-N2-O2 ~ 204 5,89 Trp 19-) Tirozin C9-H7-N-O3 ~ 181 5,66 Tyr 20-) Valin C5-H11-N-O2 117 5,96 Val Tablomuzda, doğada en çok bulunan 20 tane amino asitin kimyasal formülleri ve özellikleri verilmiştir  Bunun yanında bilinmeyen amino asitlerde vardır Bunun yanında bilinmeyen amino asitlerde vardır Bir kaç örnek verelim ; Bir kaç örnek verelim ;Hidroksiprolin, metilizin, fosfoserini iyodotronin vs  gibi gibi Fakat bu amino asitler ender rastlanan amino asitler olup hücre içinde en çok rastlanılanları tabloda verdiğimiz 20 tanesidir Fakat bu amino asitler ender rastlanan amino asitler olup hücre içinde en çok rastlanılanları tabloda verdiğimiz 20 tanesidir Amino asitler üzerlerinde belirli miktarlarda elektrik yükü taşırlar  Bu elektrik yükleri (+ veya -), asit veya baz özelliği gösteren bir ortama girdiklerinde nötrleşmeye başlarlar Bu elektrik yükleri (+ veya -), asit veya baz özelliği gösteren bir ortama girdiklerinde nötrleşmeye başlarlar Fakat bu nötrleşme ortamın pH ' ına bağlıdır Fakat bu nötrleşme ortamın pH ' ına bağlıdır Bir amino asit ancak belirli bir pH noktasında nötr hale gelebilir ki bu pH seviyesine o amino asitin " İzoelektrik noktası " denir Bir amino asit ancak belirli bir pH noktasında nötr hale gelebilir ki bu pH seviyesine o amino asitin " İzoelektrik noktası " denir Örneğin Histidin amino asiti, ancak pH ' ı 7,47 olan bir sıvı içerisinde nötr hale gelebilir Örneğin Histidin amino asiti, ancak pH ' ı 7,47 olan bir sıvı içerisinde nötr hale gelebilir Yani bazik bir ortamda Yani bazik bir ortamda Dikkat edilecek en önemli nokta moleküllerdeki atomlardır  Bu atomlardan C (karbon), N (azot) ve H (hidrojen) molekülün yapısına en çok giren atomlardır Bu atomlardan C (karbon), N (azot) ve H (hidrojen) molekülün yapısına en çok giren atomlardır Fakat aralarındaki en önemli atom ise karbon atomudur Fakat aralarındaki en önemli atom ise karbon atomudur Karbon, atom numarası 6 olan eşsiz bir yapıya sahiptir Karbon, atom numarası 6 olan eşsiz bir yapıya sahiptir Doğada saf olarak grafit ve elmas halinde bulunan karbonun yapısına girmediği bileşik hemen hemen yok gibidir Doğada saf olarak grafit ve elmas halinde bulunan karbonun yapısına girmediği bileşik hemen hemen yok gibidir Bu özelliği sayesinde yüzbinlerce kimyasal bileşik oluşturduğu bilinmektedir Bu özelliği sayesinde yüzbinlerce kimyasal bileşik oluşturduğu bilinmektedir Elimizdeki deriden arabalarımızın lastiklerine, bilgisayarımızdan ayakkabılarımıza kadar her yerde karbonlu bileşikler vardır Elimizdeki deriden arabalarımızın lastiklerine, bilgisayarımızdan ayakkabılarımıza kadar her yerde karbonlu bileşikler vardır İkinci dikkat edilecek nokta ise lösin ve izolösin amino asitlerin molekül formülleri ve molekül ağırlıkları birbirinin aynı olmasına rağmen isimlerinin farklı olmasıdır  Bunun nedeni ise bu moleküllerin 3 boyutlu yapılarının birbirinden farklı olmasıdır Bunun nedeni ise bu moleküllerin 3 boyutlu yapılarının birbirinden farklı olmasıdır Lösin ve izolösin, doğada var olan amino asitlerin D ve L konfigürasyonlarına bir örnektir  Çünki doğada amino asitler iki konfigürasyonda bulunabilirler Çünki doğada amino asitler iki konfigürasyonda bulunabilirler Bunlardan birinci konfigürasyon D, ikinci konfigürasyon ise L adını alır Bunlardan birinci konfigürasyon D, ikinci konfigürasyon ise L adını alır Bu şekilde adlandırılmasının nedeni, aynı yapıya ve formüle sahip moleküllerin arasındaki farkın yanlızca H ve 0H atomlarının yerlerinin değişik olmasından dolayıdır Bu şekilde adlandırılmasının nedeni, aynı yapıya ve formüle sahip moleküllerin arasındaki farkın yanlızca H ve 0H atomlarının yerlerinin değişik olmasından dolayıdır 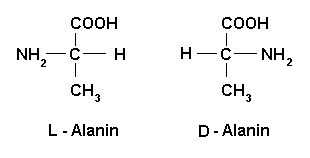 Şekilde " Alanin " amino asitinin doğada bulunan iki konfigürasyonunu görmektesiniz Şekilde " Alanin " amino asitinin doğada bulunan iki konfigürasyonunu görmektesiniz Her iki molekülün yapısı aynı olmasına karşın H ve NH2 (amino grubu) molekülünün yerleri değişiktir  Bu şekilde özellik gösteren yani kapalı formülleri aynı fakat üç boyutları farklı olan moleküllere " İzomer " molekülleri adı verilir Bu şekilde özellik gösteren yani kapalı formülleri aynı fakat üç boyutları farklı olan moleküllere " İzomer " molekülleri adı verilir Canlı organizmaların yapısında ise yanlızca L konfigürasyonundaki amino asitler bulunmuş olup çok ender olarak bazı hücrelerde D konfigürasyonuna sahip amino asitlerede rastlanılmıştır  Amino asit molekülleri, bir ucunda " Amino grubu (NH2) " diğer ucunda ise " Karboksil (COOH) " grubu taşırlar  İşte amino asitlerin yan yana gelip zincirler oluşturarak proteinleri sentezlemesi, bu iki grubun aralarında kovalent veya iyonik bağ yapmasıyla gerçekleşir İşte amino asitlerin yan yana gelip zincirler oluşturarak proteinleri sentezlemesi, bu iki grubun aralarında kovalent veya iyonik bağ yapmasıyla gerçekleşir İki amino asit yan yana geldiklerinde COOH ve NH2 grupları arasında bağlanma meydana gelir ve bu bağa " Peptid " bağı adı verilir  Bağlanma sırasında ise bir su molekülü sebest kalır Bağlanma sırasında ise bir su molekülü sebest kalır İki amino asitin yanlızca uç kısımlarını yani karboksil ve amino gruplarının nasıl bağlandını birde reaksiyon şeklinde görelim İki amino asitin yanlızca uç kısımlarını yani karboksil ve amino gruplarının nasıl bağlandını birde reaksiyon şeklinde görelim COOH + NH2 <--------------------> CO -- NH + H2O (su) Denklemimizde COOH 1  aminoasitin bir ucu, NH2 ise 2 aminoasitin bir ucu, NH2 ise 2 amino asitimizin diğer ucunu temsil etmektedir amino asitimizin diğer ucunu temsil etmektedir Bu uçlar yanyana geldiklerinde COOH grubundan bir oksijen ve NH2 grubundan bir hidrojen serbest kalır Bu uçlar yanyana geldiklerinde COOH grubundan bir oksijen ve NH2 grubundan bir hidrojen serbest kalır Böylelikle serbest kalan bu atomlar aralarında bağ yaparak suyu oluşturur Böylelikle serbest kalan bu atomlar aralarında bağ yaparak suyu oluşturur CO ile NH arasındaki bağ ise " Peptid " bağıdır  İki amino asitin yanyana gelmesiyle oluşan peptid bağına İki amino asitin yanyana gelmesiyle oluşan peptid bağına" Dipeptid", üç veya daha fazla (yüzlerce yada binlerce) amino asitin yanyana gelmesiyle oluşan zincirdeki peptid bağlarına ise " Polipeptid " adı verilir  Proteinler düz amino asit zincirlerinden meydana gelmesine rağmen oldukça karmaşık yapılara sahiptir  Bunun nedeni ise zincirdeki bazı amino asitlerin birbirleriyle ikinci veya üçüncü bir bağ yapmasındandır Bunun nedeni ise zincirdeki bazı amino asitlerin birbirleriyle ikinci veya üçüncü bir bağ yapmasındandır (Bkz (Bkz Temel bilgiler sayfası "Proteinler" bölümü) Temel bilgiler sayfası "Proteinler" bölümü) Proteinler hücre için mutlaka gerekli moleküller olup bazı proteinler enzim yapısındadırlar ve hücre içerisinde sürekli olarak kimyasal reaksiyon basamaklarına katılarak metabolik faaliyetleri düzenlerler Proteinler hücre için mutlaka gerekli moleküller olup bazı proteinler enzim yapısındadırlar ve hücre içerisinde sürekli olarak kimyasal reaksiyon basamaklarına katılarak metabolik faaliyetleri düzenlerler Hücre amino asitleri yan yana getirip proteinleri sentezlediği gibi aynı şekilde vücuda alınan proteinleride en küçük birimlerine kadar ayırır  Örneğin gıda olarak tüketilen et, yumurta, süt ve yoğurt gibi besinler bol miktarda protein içerir Örneğin gıda olarak tüketilen et, yumurta, süt ve yoğurt gibi besinler bol miktarda protein içerir Fakat hücrelerin her zaman proteine ihtiyacı olmaz ve bu proteinleri amino asitlerine kadar parçalarlar Fakat hücrelerin her zaman proteine ihtiyacı olmaz ve bu proteinleri amino asitlerine kadar parçalarlar Moleküllerin vücuda alındıktan sonra parçalanması olayına " Katabolizma ", vücuttaki küçük moleküllerden daha büyük başka moleküller sentezlenmesi olayına ise " Anabolizma " denir  Proteinlerin Yapısı Ve Yıkımı Proteinler fiziksel yapıları itibariyle iki ana gruba ayrılırlar  Birinci grup " fibröz " proteinlerdir  Bu proteinler özellikle deri, tendon (kasları kemiğe bağlayan sert doku) ve kemik dokularda bulunur Bu proteinler özellikle deri, tendon (kasları kemiğe bağlayan sert doku) ve kemik dokularda bulunur Fibröz protein suda çözünmemekle birlikte fiziksel olarak oldukça dayanıklı bir yapıya sahiptir Fibröz protein suda çözünmemekle birlikte fiziksel olarak oldukça dayanıklı bir yapıya sahiptir İkinci grup ise " Globular " proteinlerdir  Globular proteinlerde fibröz proteinin aksine suda çözünebilirler ve fiziksel olarak dayanıklı değillerdir Globular proteinlerde fibröz proteinin aksine suda çözünebilirler ve fiziksel olarak dayanıklı değillerdir Globular proteinler ekseri olarak " Enzim " yapısındadırlar Globular proteinler ekseri olarak " Enzim " yapısındadırlar Enzimler ise hücre içerisindeki sitoplazmada kimyasal reaksiyonarı katalizlerler Enzimler ise hücre içerisindeki sitoplazmada kimyasal reaksiyonarı katalizlerler Bunun yanı sıra proteinler 3 boyutlu yapıları itibariyle dört farklı konfigürasyonda bulunurlar  Bu konfigürasyonlar sırasıyla ;
Bir proteinin primer yapısı yanlızca amino asit moleküllerinin yan yana gelip zincir oluşturmalarından ibarettir  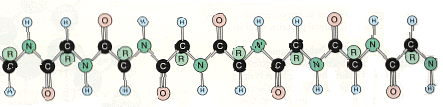 Şekildede gördüğünüz gibi polpeptid zinciri yanlızca amino asit moleküllerinin yan yana dizilmesinden oluşmaktadır  Yapıda R harfiyle gösterilen bölge " Radikal " grubunu temsil ediyor olup amino asitten amino asite bu molekül grubu değişmektedir Yapıda R harfiyle gösterilen bölge " Radikal " grubunu temsil ediyor olup amino asitten amino asite bu molekül grubu değişmektedir Mesela Alanin amino asitinde R grubu CH3 yani metil grubudur  Fakat İyodotronin amino asitinde metil grubunun yerini iyotlu bir bileşik alır Fakat İyodotronin amino asitinde metil grubunun yerini iyotlu bir bileşik alır 2-) Segonder yapı : Segonder yapı, primer yapıdan sonra gelen biraz daha kompleks bir yapıdır  Bu yapı tıpkı DNA zinciri gibi heliks dönümleri yapar ki bu şeklinede Alfa - heliks adı verilir Bu yapı tıpkı DNA zinciri gibi heliks dönümleri yapar ki bu şeklinede Alfa - heliks adı verilir 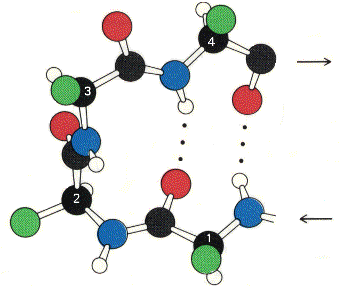 Şekilde Alfa - heliks kıvrılmasının ilk aşamasını görmektesiniz Şekilde Alfa - heliks kıvrılmasının ilk aşamasını görmektesiniz Bu aşamada zincir bükülmeye başlar ve COOH yani karbonil grubu ile NH' yani amino grubu arasında H bağı oluşmaya başlar Bu aşamada zincir bükülmeye başlar ve COOH yani karbonil grubu ile NH' yani amino grubu arasında H bağı oluşmaya başlar Bu bağ fiziksel olarak kuvvetli bir bağ değildir ve dışarıdan verilen ısı veya fiziksel bir hareket ile koparılabilir  Kopmanın etkisiyle zincir yine eski düz halini almaya başlar Kopmanın etkisiyle zincir yine eski düz halini almaya başlar Heliks yapısındaki bir zincirin enerji verilerek düz zincir haline gelmesi olayına " Denatürasyon " denir  Isı veya kimyasal etkiler ortadan kaldırılınca düz zincirin tekrar heliks yapısını kazanması olayına ise " Renatürasyon " denir Isı veya kimyasal etkiler ortadan kaldırılınca düz zincirin tekrar heliks yapısını kazanması olayına ise " Renatürasyon " denir Fakat proteinler yapılarının bozulması için verilen ısıya belli bir dereceye kadar tolerans gösterebilir  Yaklaşık 60 derecenin üstünde bir sıcaklık uygulanırsa protein denatüre olduktan sonra tekrar renatüre olamaz Yaklaşık 60 derecenin üstünde bir sıcaklık uygulanırsa protein denatüre olduktan sonra tekrar renatüre olamaz 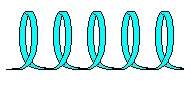 Zincir yukarıdaki şekilde gösterildiği gibi kıvrılmaya başladıktan sonra yandaki gibi heliks halini almaya başlar Zincir yukarıdaki şekilde gösterildiği gibi kıvrılmaya başladıktan sonra yandaki gibi heliks halini almaya başlar Proteinlerin önce düz zincir halinde oluşmaları ve daha sonra heliks yapısını kazanmaları tamamen enzimatik kontrol altındadır  Eğer üretilecek protein bir enzim olacaksa, enzimden enzim üretme gibi bir durum ortaya çıkmaktadır   Soldaki şekilde görülen yapı ise proteinin segonder formunun daha değişik bir şekli olan ve ß - tabakası adı verilen bir konfigürasyondur Soldaki şekilde görülen yapı ise proteinin segonder formunun daha değişik bir şekli olan ve ß - tabakası adı verilen bir konfigürasyondur Bu konfigürasyonda primer zinciri meydana getiren amino asitler heliks yapmak yerine kıvrılmalar yaparak akordiyon gibi bir hal almıştır Bu konfigürasyonda primer zinciri meydana getiren amino asitler heliks yapmak yerine kıvrılmalar yaparak akordiyon gibi bir hal almıştır Proteinler ayrı ayrı konfigürasyonlara sahip olabildiği gibi her iki konfigürasyona sahip proteinlerde vardır Proteinler ayrı ayrı konfigürasyonlara sahip olabildiği gibi her iki konfigürasyona sahip proteinlerde vardır Örneğin bazı proteinlerin % 70 ' i Segonder Alfa - heliks yapısından, geri kalan % 30 ' nu ise segonder ß - tabakasından meydana gelebilir  3-) Tersiyer yapı : Segonder yapıyı takip eden bu konfigürasyonda proteinin yapısı dahada kompleks bir hal almaya başlar  Tersiyer yapı ise, amino asitlerin yukarıda belirttiğimiz R (radikal) yan zincirleri arasında meydana gelen bağlar ile şeklini kazanmaya başlar Tersiyer yapı ise, amino asitlerin yukarıda belirttiğimiz R (radikal) yan zincirleri arasında meydana gelen bağlar ile şeklini kazanmaya başlar  Tersiyer yapı segonder yapının kıvrılmış halidir Tersiyer yapı segonder yapının kıvrılmış halidir Segonder yapı içerisinde heliks düzeni ve beta düzeninin her ikiside bulunabilir Segonder yapı içerisinde heliks düzeni ve beta düzeninin her ikiside bulunabilir Hatta bunlara ilave olarak bazı bölgeler, primer ve Hatta bunlara ilave olarak bazı bölgeler, primer ve" Kangal " adı verilen daha değişik konfigürasyonlara sahip olabilir  Protein zincirinin R yan molekülleri arasındaki bağlar ise iyonik, disülfit, H bağı ve hidrofobik (su sevmeyen) bağları olabilir  4-) Kuaterner yapı : En karmaşık şekillere sahip olan kuaterner konfigürasyonundaki proteinler, şekillerini, alt birimler olan radikal ve diğer gruplara bağlı diğer alt gruplar arasındaki bağlar ile kazanır   Şekilde kuaterner yapıda bir protein görülyüyor Şekilde kuaterner yapıda bir protein görülyüyor Polipeptid (protein) zincrlerini meydana getiren amino asitlere bağlı R gruplarının kendileride alt birimlere ayrılırlar  Kuaterner yapıyı meydana getiren yapı ise, bu alt grupların arasında meydana gelen iyonik veya H (hidrojen) bağları ile şekillenir Kuaterner yapıyı meydana getiren yapı ise, bu alt grupların arasında meydana gelen iyonik veya H (hidrojen) bağları ile şekillenir Kuaterner yapıya sahp proteinler oldukça karmaşık olmasına karşın enzimler tarafından titizlikle meydana getirilmiş mükemmel moleküllerdir  Enzimlerin en ilginç görevleride şüphesiz protein sentezlerinde üstlendikleri görevlerdir  Birincil enzimler primer yapıyı meydana getirdikten sonra devreye ikincil enzimler girer ve primer dizisini sanki matematik hesabı yapmayı biliyorlarmış gibi belirli sıralar atlayarak birbirine bağlamaya başlarlar Birincil enzimler primer yapıyı meydana getirdikten sonra devreye ikincil enzimler girer ve primer dizisini sanki matematik hesabı yapmayı biliyorlarmış gibi belirli sıralar atlayarak birbirine bağlamaya başlarlar Örneğin birinci amino asitin R grubunu, 4 amino asit sırası atlayarak 5 Örneğin birinci amino asitin R grubunu, 4 amino asit sırası atlayarak 5 amino asite bağlaması gibi amino asite bağlaması gibi Devreye başka başka enzimler girerek en sonunda proteini tersiyer ve kuaterner yapısına kavuştururlar  Sadece bir molekül olan enzimlerin bu mükemmel görevi kusursuz bir biçimde yerine getirmesi, küçük bir dev olan hücre içerisindeki mucizelerden yanlızca birisidir Sadece bir molekül olan enzimlerin bu mükemmel görevi kusursuz bir biçimde yerine getirmesi, küçük bir dev olan hücre içerisindeki mucizelerden yanlızca birisidir Proteinlerin yıkımı : Polipeptid zincirleri çok uzun olup yıkılmaları yine enzimler vasıtasıyla olur  Peptid bağlarını kıran enzim ise Peptid bağlarını kıran enzim ise" Peptidaz " enzimidir  Proteinlerin ayrılma işlemine ise " Hidroliz " denir  Protein zincirleri " Tam hidroliz " yada " Tam olmayan hidroliz " yoluyla parçalanırlar Protein zincirleri " Tam hidroliz " yada " Tam olmayan hidroliz " yoluyla parçalanırlar Tam hidroliz işlemiyle proteinler, kendilerini meydana getiren amino asitlere kadar ayrılırlar Tam hidroliz işlemiyle proteinler, kendilerini meydana getiren amino asitlere kadar ayrılırlar Fakat tam olmayan hidroliz işlemiyle proteinler belirli uzunluklarda kesilirler Fakat tam olmayan hidroliz işlemiyle proteinler belirli uzunluklarda kesilirler 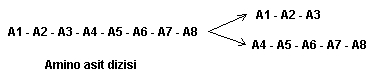 Şekilde tam olmayan hidroliz olayına bir örnek verilmiştir  8 amino asitlik bir polipeptid zinciri, tam olmayan hidrolizle yıkıma uğratılarak biri 3 amino asitten, diğeri 8 amino asitten oluşan iki ayrı zincire ayrılmıştır 8 amino asitlik bir polipeptid zinciri, tam olmayan hidrolizle yıkıma uğratılarak biri 3 amino asitten, diğeri 8 amino asitten oluşan iki ayrı zincire ayrılmıştır Proteinlerin parçalanması ve sindirilmesi ise mide de gerçekleşir  Midede çalışan enzimler, ancak pH ' ı 1 - 2 gibi çok asidik ortamlarda aktivite gösterebilirler Midede çalışan enzimler, ancak pH ' ı 1 - 2 gibi çok asidik ortamlarda aktivite gösterebilirler Bu yüzden mide çeperindeki özelleşmiş salgılama hücreleri pepsin adı verilen asit tabiatlı bir sıvı salgılar ki bu sıvı mide sıvısının pH 2 ını enzimlerin çalışacağı noktaya, yani pH ' ı Bu yüzden mide çeperindeki özelleşmiş salgılama hücreleri pepsin adı verilen asit tabiatlı bir sıvı salgılar ki bu sıvı mide sıvısının pH 2 ını enzimlerin çalışacağı noktaya, yani pH ' ı1 - 2 seviyesine kadar düşürür  Mide bu derece güçlü asidik bir sıvıya yataklık yapmasına rağmen zarar görmez çünki mideye zarar gelmemesi için mükemmel bir şekilde önlem alınmıştır  Yine mide çeperlerinde bulunan özelleşmiş salgı hücreleri, mukus adı verilen bir tür sıvı salgılarlar Yine mide çeperlerinde bulunan özelleşmiş salgı hücreleri, mukus adı verilen bir tür sıvı salgılarlar Bu sıvı asitli ortam ile mide arasında bir kalkan gibi ödev görerek mideyi korur Bu sıvı asitli ortam ile mide arasında bir kalkan gibi ödev görerek mideyi korur Sakkarit (şeker) Metabolizması Şeker molekülleri, karbonhidrat adı verilen uzun zincirli moleküllerin yapıtaşlarını meydana getirirler  Şeker molekülleri genelde 6 karbonlu bir yapıya sahip olup tıpkı amino asitler gibi D ve L konfigürasyonlarına sahiptir Şeker molekülleri genelde 6 karbonlu bir yapıya sahip olup tıpkı amino asitler gibi D ve L konfigürasyonlarına sahiptir Şeker molekülü tek başına bulunduğu hallerde " Monosakkarit ", ikili bulunduğu hallerde " Disakkarit ", 3 lü veya daha fazla gruplar halinde bulundukları zaman ise " Polisakkarit " adını alır  Öncelikle bir şeker molekülünün yapısını inceleyelim Öncelikle bir şeker molekülünün yapısını inceleyelim 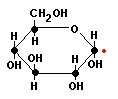 Yandaki şekilde görüldüğü gibi " Glikoz ", yapısında toplam 6 adet karbon atomu (siyah noktalar) içerir Yandaki şekilde görüldüğü gibi " Glikoz ", yapısında toplam 6 adet karbon atomu (siyah noktalar) içerir Sırasıyla tüm karbonlara H ve OH molekülleri, birbirlerine zıt yönde bağlanma göstermişlerdir Sırasıyla tüm karbonlara H ve OH molekülleri, birbirlerine zıt yönde bağlanma göstermişlerdir Molekülün 1  karbonu kırmızı noktanın hemen yanındaki karbondur karbonu kırmızı noktanın hemen yanındaki karbondur Hemen altındaki karbon ise 2 Hemen altındaki karbon ise 2 karbondur karbondur Molekülün 6 Molekülün 6 karbonu ise CH2-OH molekülünün karbonudur karbonu ise CH2-OH molekülünün karbonudur O ile gösterilen ilk sıradaki atom ise oksijendir O ile gösterilen ilk sıradaki atom ise oksijendir Molekülümüz bir monosakkaritdir Molekülümüz bir monosakkaritdir Disakkarit ve polisakkaritler bunun gibi yüzlerce yada binlerce glikoz (veya fruktoz, sukroz, laktoz vs Disakkarit ve polisakkaritler bunun gibi yüzlerce yada binlerce glikoz (veya fruktoz, sukroz, laktoz vs olabilir) molekülünün yan yana gelip bağ yapmasıyla meydana gelir olabilir) molekülünün yan yana gelip bağ yapmasıyla meydana gelir Şeker molekülleri arasındaki bağlar ise tıpkı amino asitlerde olduğu gibi kuyruk ve baş bölgelerinde meydana gelir  İki şeker molekülü bağ yaparken (örneğimizde glikoz molekülünü ele alıyoruz), kırmızı nokta ile gösterilen 1  karbonun üzerindeki H atomu ile 2 karbonun üzerindeki H atomu ile 2 glikoz molekülünün 4 glikoz molekülünün 4 karbonunun (yani kırmızı noktanın tam karşısına gelen bölgedeki karbon atomunun) altındaki OH molekülü ile bağ yapar karbonunun (yani kırmızı noktanın tam karşısına gelen bölgedeki karbon atomunun) altındaki OH molekülü ile bağ yapar Bu bağa ise " Glikozidik " bağı adı verilir Bu bağa ise " Glikozidik " bağı adı verilir Glikoz molekülleri bu şekilde ardarda bağ yaparak karbohidrat zincirlerini meydana getirirler Glikoz molekülleri bu şekilde ardarda bağ yaparak karbohidrat zincirlerini meydana getirirler Şeklimizde görülen glikoz molekülü Alfa - Glikoz adını alır  Molekülün Alfa veya Beta olması ise 1 Molekülün Alfa veya Beta olması ise 1 karbondaki H ve OH ın konumlarına bağlıdır karbondaki H ve OH ın konumlarına bağlıdır Eğer H atomu karbounun alt tarafından bağ yapmış ise molekülümüz Beta konfigürasyonu, üst taraftan bağ yapmış ise Alfa konfigürasyonu adını alır Eğer H atomu karbounun alt tarafından bağ yapmış ise molekülümüz Beta konfigürasyonu, üst taraftan bağ yapmış ise Alfa konfigürasyonu adını alır Şekerlerin 5 karbon atomundan oluşan formlarıda vardır  5 karbon atomu içeren şeker molekülüne ise " Pentoz " adı verilir 5 karbon atomu içeren şeker molekülüne ise " Pentoz " adı verilir Bunların dışında değişik yapılara sahip şeker moleküllerine örnek olarak mannoz, sukroz, laktoz ve fruktoz örnek verilebilir Bunların dışında değişik yapılara sahip şeker moleküllerine örnek olarak mannoz, sukroz, laktoz ve fruktoz örnek verilebilir Şeker moleküllerinin yıkımı : Karbonhidratların büyük çoğunluğunun uzun şeker moleküllerinden meydana geldiğini belirtmiştik  Vücuda alınan besin maddelerinin ise % 70 e yakını karbonhidratlardan meydana gelir Vücuda alınan besin maddelerinin ise % 70 e yakını karbonhidratlardan meydana gelir Karbonhidratların sindirimi ağızda başlar  Tükürük sıvısında karbonidrat zincirlerini parçalayan enzimler bulunmaktadır Tükürük sıvısında karbonidrat zincirlerini parçalayan enzimler bulunmaktadır Kısmen parçalanan bu moleküllerin sindirimi ise ince bağırsakta sonlanır Kısmen parçalanan bu moleküllerin sindirimi ise ince bağırsakta sonlanır Şeker molekülleri kana karıştıktan sonra kan basıncının yükselmesine neden olur Şeker molekülleri kana karıştıktan sonra kan basıncının yükselmesine neden olur Fakat kan basıncı, glikoz molekülüne müdahele eden enzimler vasıtasıyla dengede tutulur Fakat kan basıncı, glikoz molekülüne müdahele eden enzimler vasıtasıyla dengede tutulur Şeker molekülleri monosakkarit formları şeklinde bağırsaklardan emildikten sonra kan yoluyla karaciğere gider  Monosakkaritler burada glikoz, fruktoz, mannoz gibi değişik yapıdaki şeker moleküllerine çevrlirler Monosakkaritler burada glikoz, fruktoz, mannoz gibi değişik yapıdaki şeker moleküllerine çevrlirler Glikoz moleküllerinin fazlası ise enzimler vasıtasıyla " Glikojen " adı verilen başka bir şekle dönüştürülüp depo edilir Glikoz moleküllerinin fazlası ise enzimler vasıtasıyla " Glikojen " adı verilen başka bir şekle dönüştürülüp depo edilir Glikozun glikojene çevrilmesinde rol oynayan enzimin adı ise " Glikokinaz " enzimidir  Bu enzim karaciğer tarafından üretilir ve bu üretim, pankreastan salınan ve " İnsülin " adı verilen bir hormonun kontrolü altındadır Bu enzim karaciğer tarafından üretilir ve bu üretim, pankreastan salınan ve " İnsülin " adı verilen bir hormonun kontrolü altındadır Glikokinaz (enzim) --------> Glikoz (molekül) --------> Glikojen (son ürün) Eğer bir insanın pankreası yeteri kadar insülin hormonu salgılayamıyorsa, kişinin karaciğeri, kandaki insülin miktarının azalmasına paralel olarak yeteri kadar Glikokinaz enzimi üretemez  Glikokinaz enzimi ise glikoz moleküllerine müdahele edemeyince glikoz moleküllerinin kandaki miktarı süratle artmaya başlar Glikokinaz enzimi ise glikoz moleküllerine müdahele edemeyince glikoz moleküllerinin kandaki miktarı süratle artmaya başlar Glikozun kanda artış göstermesi nedeniyle kan basıncı artmaya başlar ve sonunda yüksek tansiyon denilen rahatsızlık ortaya çıkar Glikozun kanda artış göstermesi nedeniyle kan basıncı artmaya başlar ve sonunda yüksek tansiyon denilen rahatsızlık ortaya çıkar Glikozun parçalanması kısaca şu şekilde meydana gelir ; 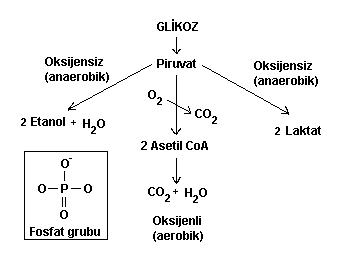 6 karbonlu glikoz molekülü, yapılarında 3 er tane karbon atomu bulunduran 2 molekül Piruvat ' a dönüşür 6 karbonlu glikoz molekülü, yapılarında 3 er tane karbon atomu bulunduran 2 molekül Piruvat ' a dönüşür Piruvat, ortamda oksijen olma veya olmama durumuna göre 2 yol izleyebilir Piruvat, ortamda oksijen olma veya olmama durumuna göre 2 yol izleyebilir Eğer ortamda oksijen yoksa (anaerob) piruvat molekülleri son ürün olarak Laktat ve daha sonra Laktik asit ' e dönüşür  Laktik asit, kaslara yeteri kadar oksijen taşınamadığı hallerde birikir ve yorgunluğa neden olur Laktik asit, kaslara yeteri kadar oksijen taşınamadığı hallerde birikir ve yorgunluğa neden olur Fakat fermantasyon bakterileri ve bazı maya türleri, ortamda oksijen olmadığı hallerde laktat yerine Etanol adını alan bir çeşit alkol ve su üretirler  Eğer ortamda oksijen varsa (aerob) Piruvat oksijenle reaksiyona girerek öncelikle bir ara ürün olan Asetil CoA ' ya dönüşür  Asetil CoA ara ürünü daha sonra sitrik asit halkası adı verilen bir seri kimyasal reaksiyon basamaklarına girer ve nihayetinde son ürün olarak karbondioksit ve su ya dönüşür  Glikoz moleküllerinin parçalanma reaksiyonları sırasında hücre ATP kazanır  ATP ise enerji gereksinimleri için kimyasal reaksiyonlarda kullanılır ATP ise enerji gereksinimleri için kimyasal reaksiyonlarda kullanılır Glikozun tam yıkım reaksiyon şemasını aşağıdaki ikona tıklayarak görüntüleyebilirsiniz Glikozun tam yıkım reaksiyon şemasını aşağıdaki ikona tıklayarak görüntüleyebilirsiniz Tam reaksiyon şeması için Buraya tıklayın Moleküller adlandırılırken aralarına tire konularak, hangi radikalin kaçıncı karbona bağlı olduğuda virgüllerle belirtilir  Örnek verelim ; Örnek verelim ;Bir molekül " Glikoz - 6 - Fosfat " olarak isimlendirilmiş ise, bu, molekülün 6  karbonunda bir tane fosfat grubu taşıdığı gösterir karbonunda bir tane fosfat grubu taşıdığı gösterirBaşka bir örnek olarak ; Eğer molekül " Fruktoz - 1,6 - Difosfat " olarak isimlendirilmiş ise, buda Fruktoz molekülünün 1  ve 6 ve 6 karbon atomlarının Fosfat molekülü taşıdığı anlamına gelir karbon atomlarının Fosfat molekülü taşıdığı anlamına gelir Fruktoz üzerinde toplam 2 tane fosfat grubu olduğundan " Difosfat " olarak yazılır Fruktoz üzerinde toplam 2 tane fosfat grubu olduğundan " Difosfat " olarak yazılır Glikoz yıkıma uğrarken, hem parçalanmakta hemde bazı karbon atomlarına fosfat ve diğer kimyasal gruplar eklenmektedir (Bu eklenmeler " Tam reaksiyon şeması " ' nda ayrıntılı olarak gösterilmektedir)  Bu kısa bilgiden sonra Glikozun yıkımı sırasında hangi basamaklarda ATP harcandığını ve hangi basamaklarda ATP üretildiğini görelim  Reaksiyon ATP değişimi Glikoz ---> Glikoz - 6 - fosfat - 1 ATP Fruktoz - 6 - fosfat ---> Fruktoz - 1,6 - difosfat - 1 ATP 1,3 - bifosfogliserat ---> 3 - fosfogliserat + 2 ATP Fosfoenol piruvat ---> Piruvat + 2 ATP Tabloda görüldüğü gibi glikoz ve fruktoz moleküllerine fosfat bağlanırken enerji kullanılmaktadır  Bu enerji gereksinimi 2 ATP yi beraberinde götürürken, fosfat gruplarının ayrılması esnasında 2 şer adet ATP kazanılmaktadır Bu enerji gereksinimi 2 ATP yi beraberinde götürürken, fosfat gruplarının ayrılması esnasında 2 şer adet ATP kazanılmaktadır Sonuç olarak harcanan 2 ATP ye karşın hücrede 4 ATP üretilmekte ve net olarak 2 ATP kazanç sağlamaktadır Sonuç olarak harcanan 2 ATP ye karşın hücrede 4 ATP üretilmekte ve net olarak 2 ATP kazanç sağlamaktadır Glikozun metabolik faaliyetlerle yıkılması olayına " Glikoliz ", küçük moleküllerden tekrar sentezlenmesi olayına ise " Glikogenez " denir  Vücuda yeteri kadar glikoz alınmaz ise hücreler bu sefer glikoz üretmeye başlarlar Vücuda yeteri kadar glikoz alınmaz ise hücreler bu sefer glikoz üretmeye başlarlar Yağ (Lipid) Metabolizması Besinlerle alınan yağ moleküllerinin büyük kısmını trigliserid adı verilen moleküller oluşturmaktadır  Bunun yanında fosfolipid, ve kolestrol molekülleri yağlı besinlerde daha az miktarlarda bulunular Bunun yanında fosfolipid, ve kolestrol molekülleri yağlı besinlerde daha az miktarlarda bulunular Lipidler yapı itibariyle gliserin ve yağ asitlerinin teşkil ettiği moleküllerdir  Lipid molekülleri hidrofobik özellik göstermelerine karşın organik eriticilerde çözünürler Lipid molekülleri hidrofobik özellik göstermelerine karşın organik eriticilerde çözünürler Örneğin alkol, eter, aseton ve klorofom gibi uçucu sıvılar içerisinde çözünebilir Örneğin alkol, eter, aseton ve klorofom gibi uçucu sıvılar içerisinde çözünebilir Yağ molekülleri çok uzun bir yapıya sahip olup, biri " Hidrofobik " diğeri " Hidrofilik " iki kutuba sahiptir  Yağlar, vücudun ince bağırsağında pankreas ve safra kesesinden gelen enzimlerle küçük parçalara ayrılırlar Yağlar, vücudun ince bağırsağında pankreas ve safra kesesinden gelen enzimlerle küçük parçalara ayrılırlar Yağların parçalanması ise " Lipaz " adı verilen bir enzim ile olur Yağların parçalanması ise " Lipaz " adı verilen bir enzim ile olur Yağlar parçalanıp yağ asitlerine kadar ayrıştırıldıktan sonra ince bağırsaklardan emilir ve kana karışır  Yağ asitleri hücreler tarafından enerji ihtiyacını karşılamak için kullanılırlar Yağ asitleri hücreler tarafından enerji ihtiyacını karşılamak için kullanılırlar Yağ asitleri bazı hücrelerde sitoplazma içerisinde okside olarak ATP üretimine katılırken, çoğu hücrede mitokondri içerisine girerek ATP sentezlenmesini sağlar Yağ asitleri bazı hücrelerde sitoplazma içerisinde okside olarak ATP üretimine katılırken, çoğu hücrede mitokondri içerisine girerek ATP sentezlenmesini sağlar 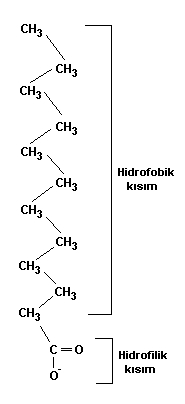 Yağ asiti moleküllerinin yapısını gösteren şekilde, molekülün hidrofilik ve hidrofobik kısımları görülmektedir Yağ asiti moleküllerinin yapısını gösteren şekilde, molekülün hidrofilik ve hidrofobik kısımları görülmektedir Yağlar vücuda girip yağ asitlerine kadar ayrıştıktan sonra ya depo edilirler yada enerji ihtiyacı için kullanılırlar  Yağ asitleri vücutta fazla miktarlarda bulunduğu zaman trigliserid şekline dönüştürüldükten sonra yağ dokularında depo edilirler  İnsanların şişmanlamasının nedenide budur İnsanların şişmanlamasının nedenide budur Fakat aksine, kaslar fazla çalıştığı zaman kas hücrelerindeki mitokondriler ATP üretmek için ortamda bulunan yağ asitlerini, depo edilmesine fırsat bırakmadan kullanırak enerji ihtiyaçlarını karşılarlar Fakat aksine, kaslar fazla çalıştığı zaman kas hücrelerindeki mitokondriler ATP üretmek için ortamda bulunan yağ asitlerini, depo edilmesine fırsat bırakmadan kullanırak enerji ihtiyaçlarını karşılarlar Şişman bir kimse elinden geldiğince spor yapıp hareket ederse, yağ dokularındaki trigliserid molekülleri, enerji gereksinimi olduğu için yağ asitlerine kadar parçalanacak ve mitokondrilere ulaştırılacaktır  Yağ asitlerinin mitokondriye girişi direk değildir  Öncelikle Asetil CoA ile bileşik kurarak " Yağ Asil - CoA " kompleksini kurar Öncelikle Asetil CoA ile bileşik kurarak " Yağ Asil - CoA " kompleksini kurar Bu aşamadan sonra hücre içerisinde bulunan ve " Kornitin " adı verilen bir enzim eşliğinde mitokondri membranından geçerek mitokondri matrix ' ine ulaşır Bu aşamadan sonra hücre içerisinde bulunan ve " Kornitin " adı verilen bir enzim eşliğinde mitokondri membranından geçerek mitokondri matrix ' ine ulaşır Yağ asidi + CoA + ATP <---------------> Yağ asil - CoA + AMP + PPi Denklemde yağ asitinin CoA (Koenzim A) ile komleks oluştururken ATP harcamaktadır  ATP enerjisi kullanılınca ATP (Adenin trifosfat) AMP (Adenin monofosfat) ' a dönüşmektedir ATP enerjisi kullanılınca ATP (Adenin trifosfat) AMP (Adenin monofosfat) ' a dönüşmektedir Yağların kan sıvısında taşınması ise ortak çalışan iki protein ile gerçekleşmektedir  Bu proteinlerden birisi Bu proteinlerden birisi" Lipoprotein " diğeri ise " Apolipoprotein " adını alır  Yiyeceklerle alınan yağ ve kolestroller önce lipoprotienler ile paketlenirler Yiyeceklerle alınan yağ ve kolestroller önce lipoprotienler ile paketlenirler Lipoprotinlerin üzerilerinde ise apolipoprotein molekülleri vardır Lipoprotinlerin üzerilerinde ise apolipoprotein molekülleri vardır Apolipoprotein ise ise lipide bağlanan kısımı oluşturmaktadır Apolipoprotein ise ise lipide bağlanan kısımı oluşturmaktadır Yani Lipoprotein apolipoproteini taşır, apolipoprotein ise yağa bağlanır Yani Lipoprotein apolipoproteini taşır, apolipoprotein ise yağa bağlanır Böylelikle yağ molekülü dokulara kan yolula taşınmış olur Böylelikle yağ molekülü dokulara kan yolula taşınmış olur Yağların yıkımı : Yağların yapıtaşlarının yağ asitleri olduğunu belirtmiştik  Yukarıdaki şekilde görülen yağ asiti molekülünün hidrofilik ve hidrofobik uçları, yağların suya döküldüklerinde misel oluşturmalarına neden olur Yukarıdaki şekilde görülen yağ asiti molekülünün hidrofilik ve hidrofobik uçları, yağların suya döküldüklerinde misel oluşturmalarına neden olur 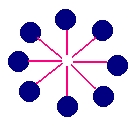 Şekilde yağ asitlerinin su içerisinde oluşturdukları micel yapısı görülmektedir Şekilde yağ asitlerinin su içerisinde oluşturdukları micel yapısı görülmektedir Yağ asitleri, hidrofilik uçları dışa, hidrofobik uçları ise iç tarafa gelecek şekilde dizilirler  Mavi bölge yağ asitinin hidrofilik bölgesi, kırmızı ince bölge ise molekülün hidrofobik kuyruğunu temsil etmektedir Mavi bölge yağ asitinin hidrofilik bölgesi, kırmızı ince bölge ise molekülün hidrofobik kuyruğunu temsil etmektedir Besinlerle alınan büyük yağ molekükleri, bağırsakta sindirilirken önce misellerine kadar ayrıştırılmakta ve daha sonra bu miselleri parçalayan enzimler iş görmektedir  İnce bağırsağa gelen büyük yağ molekülleri, öncelikle safra kesesinden salgılanan tuzlarla etkileşime girerek kendilerinden daha küçük yapıya sahip misellere dönüşürler  Bu şekilde küçültülüp misele dönen yağ molekülleri daha sonra pankreastan salgılanan lipazlar vasıtasıyla parçalanmaya ve yağ asitlerine kadar ayrışmaya başlar Bu şekilde küçültülüp misele dönen yağ molekülleri daha sonra pankreastan salgılanan lipazlar vasıtasıyla parçalanmaya ve yağ asitlerine kadar ayrışmaya başlar Ayrışan yağ asitleri difüzyon yolu ile bağırsak mikrovilluslarından emilir Ayrışan yağ asitleri difüzyon yolu ile bağırsak mikrovilluslarından emilir Fakat emilim esnasında yağ asitlerinden trigliseridler sentezlenerek bu haliyle kana karışır ve lipoproteinler vasıtasıyla paketlenerek gerekli yerlere ulaştırılır Fakat emilim esnasında yağ asitlerinden trigliseridler sentezlenerek bu haliyle kana karışır ve lipoproteinler vasıtasıyla paketlenerek gerekli yerlere ulaştırılır Dokulara ulaşan trigliseridler genel olarak 3 aşamada yıkılarak enerji ihtiyacı için kullanılırlar 
Trigliseridler Lipaz enziminin etkisiyle digliserid, monogliseridserbest gliserol ve yağ asitlerine kadar ayrışırlar  2-) Alfa - oksidasyonu : Trigliseridlerin hidrolizi ile serbest kalan yağ asitleri, alfa - oksidasyon kimyasal reaksiyonlarına girerek yıkılmaya başlar  Alfa - oksidasyonunda yağ asitleri, hücrenin Endoplazmik Retikulumunda aktive olmadan direk olarak parçalanırlar Alfa - oksidasyonunda yağ asitleri, hücrenin Endoplazmik Retikulumunda aktive olmadan direk olarak parçalanırlar 3-) Beta - oksidasyonu : Beta - oksidasyonu, yağ asitlerinin parçalandığı diğer bir kimyasal reaksiyon basamaklarıdır  Parçalanma mitokondride gerçekleşmekte ve aynı zamanda yağ asitinin Asetil - CoA ile kompleks oluşturup aktive olması gerekmektedir Parçalanma mitokondride gerçekleşmekte ve aynı zamanda yağ asitinin Asetil - CoA ile kompleks oluşturup aktive olması gerekmektedir Vücuda alınan karbonhidratlar, fruktoz, mannoz ve sukroz gibi şekerlere, glikoz şekeri ise glikojene çevrilip depo edilir  Fakat karbonhidrat fazla miktarda alınırsa bu kez glikozun fazlası glikojene çevrilemeyeceğinden, öncelikle yağ asitlerine ve daha sonrada trigliseridlere dönüştürülüp depo edilir Fakat karbonhidrat fazla miktarda alınırsa bu kez glikozun fazlası glikojene çevrilemeyeceğinden, öncelikle yağ asitlerine ve daha sonrada trigliseridlere dönüştürülüp depo edilir Hücrede aynı zamanda " Peroksizom " adı verilen yapılarda da yağ asitleri parçalanmaktadır  Peroksizomlar yağ asitlerini parçalarken ürün olarak H2O2 (Hidrojen peroksit) meydana getir Peroksizomlar yağ asitlerini parçalarken ürün olarak H2O2 (Hidrojen peroksit) meydana getir H2O2 nin fazlası hücre için toksik etki yapacağından, " Katalaz " enzimi ile parçalanarak H2O ve H2 ye dönüştürülür H2O2 nin fazlası hücre için toksik etki yapacağından, " Katalaz " enzimi ile parçalanarak H2O ve H2 ye dönüştürülür Mitokondride ise yağ asiti parçalanırken direk olarak H2O meydana gelir Mitokondride ise yağ asiti parçalanırken direk olarak H2O meydana gelir |

|
Cevap : Biyokimya (1.BÖLÜM) |
|
|
#2 |
|
Şengül Şirin

|
Cevap : Biyokimya (1.BÖLÜM)Solunum ve Fotosentez Canlı organizmalar temel olarak üç yolla enerji elde edebilirler  A-) Mitokondriyal solunum zincirileri ile  B-) Glikozun, glikozliz basamaklarında yıkılması sırasında  C-) Fotosentetik fosforilasyon ile  Mitokondri, içerisinde oldukça kompleks kimyasal reaksiyonları meydana getiren mükemmel bir organeldir  Fotosentez yapamayan canlı organizmalarda ATP üretimi kemosentez yoluyla yapılır Fotosentez yapamayan canlı organizmalarda ATP üretimi kemosentez yoluyla yapılır Yani kimyasal moleküllerin enzimlerle işlenmesiyle Yani kimyasal moleküllerin enzimlerle işlenmesiyle Fotosentez yapabilen canlılar ise ATP lerini, ışık fotonlarından absorbe ettikleri enerjiyi kullanarak sentezlerler Fotosentez yapabilen canlılar ise ATP lerini, ışık fotonlarından absorbe ettikleri enerjiyi kullanarak sentezlerler Fotosentezde ise iki devre vardır Fotosentezde ise iki devre vardır Bu devrelerden birisinde ışık kullanılırken diğerinde kullanılmaz Bu devrelerden birisinde ışık kullanılırken diğerinde kullanılmaz Solunum : Solunum ile ATP elde edilmesi üç fazda gerçekleşir  1  fazda protein, karbonhidrat ve yağları Asetil - CoA ' ya kadar parçalanır fazda protein, karbonhidrat ve yağları Asetil - CoA ' ya kadar parçalanır Bu parçalanma reaksiyonları sitoplazma içerisinde meydana gelir Bu parçalanma reaksiyonları sitoplazma içerisinde meydana gelir 2  fazda Asetil - CoA moleküllerini mitokondri matrixine girerek " Krebs " çemberine katılır fazda Asetil - CoA moleküllerini mitokondri matrixine girerek " Krebs " çemberine katılır 3  fazda ise mitokondri içerisinde Dehidrogenaz enzimleri tarafından koparılan elektronlar, elektron transfer zincirinden geçirilerek mitokondri zarında ATP sentezlenmesini sağlar fazda ise mitokondri içerisinde Dehidrogenaz enzimleri tarafından koparılan elektronlar, elektron transfer zincirinden geçirilerek mitokondri zarında ATP sentezlenmesini sağlar Solunumun ilk fazında protein, karbonhidrat, yağ ve şekerlerin nasıl yıkıma uğradıklarını en genel haliyle özetlemeye çalıştık  Şimdi ise 2 Şimdi ise 2 faz olan krebs çemberinde yıkıma uğrayan moleküllerden nasıl ATP üretildiğini şekil üzerinde görelim faz olan krebs çemberinde yıkıma uğrayan moleküllerden nasıl ATP üretildiğini şekil üzerinde görelim 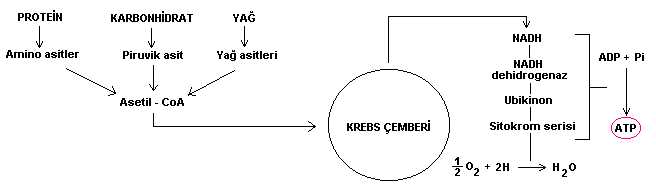 Şekilde, krebs çemberiyle birlikte solunumun en genel hali özetlenmiştir  Krebs çemberini ara ürünleriyle birlikte ayrıntılı olarak görmek için Buraya tıklayınız Solunumda özet olarak vücuda alınan yağ, karbonditrat ve proteinler Asetil - CoA ya dönüşmekte ve ardından Asetil - CoA nın krebs çemberinde enzimlerle katalizlenmesiyle ATP oluşmaktadır  Krebs çemberinde reaksiyonlar devam ederken enzimler, reaksiyona giren moleküllerden elektron (-) ve proton (H+) koparırlar Krebs çemberinde reaksiyonlar devam ederken enzimler, reaksiyona giren moleküllerden elektron (-) ve proton (H+) koparırlar 3  fazda ise mitokondriyal membranda bulunan enzimler vasıtasıyla koparılan elektron ve protonlardan ATP sentez edilir fazda ise mitokondriyal membranda bulunan enzimler vasıtasıyla koparılan elektron ve protonlardan ATP sentez edilir Membranda ATP nin nasıl sentezlendiğini şekil üzerinde görelim Membranda ATP nin nasıl sentezlendiğini şekil üzerinde görelim 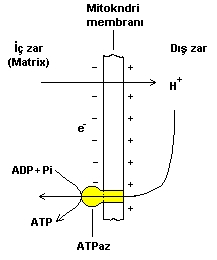 Krebs çemberinde reaksiyonlar baladıktan sonra H(+) iyonu matriksin dışarısına yani sitoplazmaya pompalanır Krebs çemberinde reaksiyonlar baladıktan sonra H(+) iyonu matriksin dışarısına yani sitoplazmaya pompalanır Çemberdeki kimyasal reaksiyonlarda koparılan elektronlar mitokondri zarının iç tarafında birikmeye başlayınca, dış zar ile iç zar arasında bir elektriksel gradiyent meydana gelir Çemberdeki kimyasal reaksiyonlarda koparılan elektronlar mitokondri zarının iç tarafında birikmeye başlayınca, dış zar ile iç zar arasında bir elektriksel gradiyent meydana gelir Bu elektrik gradiyenti H(+) iyonlarının mitokondri zarından tekrar matriks içerisine girmesine neden olur  Fakat H(+) iyonu, zarın içerisine gömülü olan kanal şeklindeki ATPaz enziminin içerisinden geçer Fakat H(+) iyonu, zarın içerisine gömülü olan kanal şeklindeki ATPaz enziminin içerisinden geçer Bu geçiş esnasında ADP (Adenin tri fosfat) molekülü yapısına bir tane daha fosfor (P) bağlayarak ATP (Adenin tri fosfat) ' ye dönüşür  ADP den ATP sentezini gerçekleştiren enzim ise ATPaz dır ADP den ATP sentezini gerçekleştiren enzim ise ATPaz dır Bu enzim, membrana bağlı bir protein olup zarın bir yüzünden diğer yüzüne kadar uzanır Bu enzim, membrana bağlı bir protein olup zarın bir yüzünden diğer yüzüne kadar uzanır Bu tip proteinlere (burada proteinimiz enzim yapısındadır) " İntegral protein " denir  Bunun dışında membrana kısmen gömülü proteinlerde vardır ki bu tip proteinlerede " Periferal protein " adı verilir Bunun dışında membrana kısmen gömülü proteinlerde vardır ki bu tip proteinlerede " Periferal protein " adı verilir Elektronların ETS (Elektron transfer zinciri) ' de taşınması ise 3 türlü olur  1-) Redoks çiftleri ile : Fe(+2) + Cu(+2) --------> Fe(+3) + Cu(+) Fe (demir) ve Cu (bakır) redoks çiftleri olup Fe ' den 1 elektron Cu ' ya geçmiştir  Redoks çiftleri arasında elektron alıp verme potansiyeline " Redoks potansiyeli " denir Redoks çiftleri arasında elektron alıp verme potansiyeline " Redoks potansiyeli " denir Elektron transfer zincirinde ise redoks çiftleri, potansiyeli küçük olandan büyük olana doğru sıralanmıştır Elektron transfer zincirinde ise redoks çiftleri, potansiyeli küçük olandan büyük olana doğru sıralanmıştır Böylelikle elektron seri bir şekilde akmaktadır Böylelikle elektron seri bir şekilde akmaktadır Redoks çiftleri ile elektron akımı, bitkilerin kloroplastlarındaki " Sitokrom " moleküllerinde de görülür Redoks çiftleri ile elektron akımı, bitkilerin kloroplastlarındaki " Sitokrom " moleküllerinde de görülür ATP ise, elektronun bir redoks çiftinden diğerine geçişi sırasında sentezlenir ATP ise, elektronun bir redoks çiftinden diğerine geçişi sırasında sentezlenir 2-) Hibrid iyonu şeklinde taşınma : 2-) Hibrid iyonu şeklinde taşınma : H + C7N2H3O -------> C7N2H40 Denklemdeki hidrojen atomu, organik bir bileşiğe bağlanarak taşınmaktadır  Fakat buradaki hidrojen atomumuz yanlızca çıplak protondan ibaret değil, (-) yükünü yani orbitalinde elektronunuda taşımaktadır Fakat buradaki hidrojen atomumuz yanlızca çıplak protondan ibaret değil, (-) yükünü yani orbitalinde elektronunuda taşımaktadır 3-) Hidrojen çiftleriyle taşınma : 3-) Hidrojen çiftleriyle taşınma :AH2 + B --------> A + BH2 Hidrojen atom çiftleri, başka atomlara veya moleküllere bağlanarak beraberlerindeki elektronlarıda bu atom veya moleküllerle ETS de taşırlar  Vücudumuza soluduğumuz oksijenin az bir kısmı kandaki oksijen bağlayıcı enzimler tarafından kullanılırken, oksijenin % 90 ' na yakını ETS de kullanılır Vücudumuza soluduğumuz oksijenin az bir kısmı kandaki oksijen bağlayıcı enzimler tarafından kullanılırken, oksijenin % 90 ' na yakını ETS de kullanılır Solunum mekanizmasında oksijen atomları, elektron alış verişinde bulunarak ETS ' nin devamlılığını sağlar Solunum mekanizmasında oksijen atomları, elektron alış verişinde bulunarak ETS ' nin devamlılığını sağlar Eğer ortamda oksijen yoksa ETS mekanizması vede dolayısıyla solunum reaksionları durur Eğer ortamda oksijen yoksa ETS mekanizması vede dolayısıyla solunum reaksionları durur Fotosentez : Canlıların enerji elde etmek için izledikleri diğer bir yol ise fotosentezdir  Fotosentezin kimyası oldukça karışıktır Fotosentezin kimyası oldukça karışıktır Fotosentezin ATP üretme sisteminin temeli, ışık enerjisinin klorofil molekülleri tarafından absorbe edilerek enerji isteyen kimyasal reaksiyonlarda kullanılması şeklindedir Fotosentezin ATP üretme sisteminin temeli, ışık enerjisinin klorofil molekülleri tarafından absorbe edilerek enerji isteyen kimyasal reaksiyonlarda kullanılması şeklindedir Yani ışık enerjisi kimyasal enerjiye dönüşmektedir Yani ışık enerjisi kimyasal enerjiye dönüşmektedir Fotosentez denklemlerini " Işık tepkimesi " ve " Karanlık tepkimesi " olmak üzere en sade haliyle aşağıdaki şekildeki gibi özetleyebiliriz  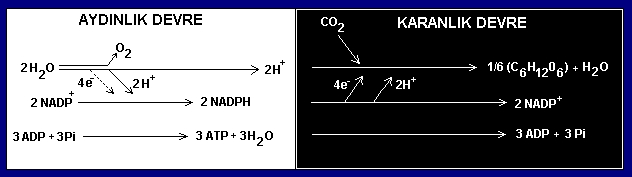 Aydınlık devrede, klorofil tarafında absorbe edilen ışık enerjisi, ATP üretiminde kullanılır  ATP üretimi için gerekli H (+) iyonları ise su moleküllerinden karşılanır ATP üretimi için gerekli H (+) iyonları ise su moleküllerinden karşılanır Suyun özel enzimlerle parçalanmasıyla açığa çıkan oksijen gazı serbest kalırken H (+) iyonları ise NADPH ve ATP üretimi için reaksiyonlara katılır Suyun özel enzimlerle parçalanmasıyla açığa çıkan oksijen gazı serbest kalırken H (+) iyonları ise NADPH ve ATP üretimi için reaksiyonlara katılır Karanlık devre, aydınlık devrede üretilen NADPH ve ATP moleküllerinin enerji gereksinimi için kullanıldığı devredir  Bu devrede ışık enerjisi rol oynamadığı için bu devreye karanlık devre denir Bu devrede ışık enerjisi rol oynamadığı için bu devreye karanlık devre denir Yani karanlık devrede yanlızca kimyasal enerji iş görmektedir Yani karanlık devrede yanlızca kimyasal enerji iş görmektedir ATP ve NADPH ların kullanımıyla elde edilen enerji, karbonhidrat ve glikoz sentezi için kullanılır (Glikozun kapalı formülü C6H12O6 dır) ATP ve NADPH ların kullanımıyla elde edilen enerji, karbonhidrat ve glikoz sentezi için kullanılır (Glikozun kapalı formülü C6H12O6 dır) Fotosentez reaksiyonları " Kloroplast " adı verilen yeşil renkli pigmentler içerisinde gerçekleşir  Bu pigmentin içerisinde en önemli yeri " Klorofil " molekülü tutmaktadır Bu pigmentin içerisinde en önemli yeri " Klorofil " molekülü tutmaktadır Klorofil, ortasında Mg (magnezyum) atomu bulunan karmaşık yapılı bir organik bileşiktir Klorofil, ortasında Mg (magnezyum) atomu bulunan karmaşık yapılı bir organik bileşiktir Kloroplastın içerisinde lamelli yapılar, bu yapıların membranlarının içerisinde ise klorofil molekülü gruplar halinde bulunurlar Kloroplastın içerisinde lamelli yapılar, bu yapıların membranlarının içerisinde ise klorofil molekülü gruplar halinde bulunurlar Bu kloforfil grupları, ışık enerjisini absorbe ettiği zaman elektron fırlatır ve asıl sentezleme işlemi bu noktadan sonra başlar Bu kloforfil grupları, ışık enerjisini absorbe ettiği zaman elektron fırlatır ve asıl sentezleme işlemi bu noktadan sonra başlar Bu karmaşık işlemlerin nasıl meydana geldiğini şekilerle görelim Bu karmaşık işlemlerin nasıl meydana geldiğini şekilerle görelim  Kloroplast şekildeki gibi kanallı bir yapıya sahiptir Kloroplast şekildeki gibi kanallı bir yapıya sahiptir Bu kanallar aslında kloroplastın çift katlı zarının iç tarafındakinin katlanmalarıyla meydana gelmiştir  Bu yassı keseciklere " Lamel ", lamellerin üst üste gelerek grup oluşturmuş haline ise " Grana " adı verilir Bu yassı keseciklere " Lamel ", lamellerin üst üste gelerek grup oluşturmuş haline ise " Grana " adı verilir Fotosentezin reaksiyonları, ince lamel (tilakoid) zarının içerisinde meydana gelir Fotosentezin reaksiyonları, ince lamel (tilakoid) zarının içerisinde meydana gelir Klorofil molekülleri lamel zarları içerisinde birbirinden bağımsız olarak konumlanmazlar  Klorofil molekülleri 200 - 300 er gruplar halinde kümelenirler ki bu kümelere " Kuantozom " adı verilir Klorofil molekülleri 200 - 300 er gruplar halinde kümelenirler ki bu kümelere " Kuantozom " adı verilir Kuantozom yani klorofil molekül grupları, ışık enerjini absorbe ederek molekül grubunun ortasında bulunan ve " P680 " olarak adlandırılan bir çeşit moleküle kadar iletir  Bu molekül klorofil molekülleri tarafından kendisine iletilen ışık enerjisinin etkisiyle elektron fırlatır Bu molekül klorofil molekülleri tarafından kendisine iletilen ışık enerjisinin etkisiyle elektron fırlatır Bundan sonraki basamakları şekil üzerinde görelim  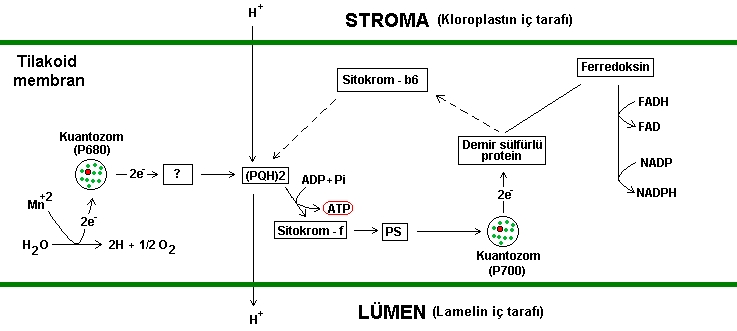 Şekildeki reaksiyonlar tilakoid zarının içerisinde cereyan etmektedir  Stroma bölgesi kloroplastın iç bölgesidir  Tilakod zar, lamelin etrafını saran zar olup lamelin iç tarafına ise Tilakod zar, lamelin etrafını saran zar olup lamelin iç tarafına ise " Lümen " denir  Işık fotonları sol tarafta görülen 1 Işık fotonları sol tarafta görülen 1 kuantozoma çarpınca (Bu kuantozom fotosistem 2 dir kuantozoma çarpınca (Bu kuantozom fotosistem 2 dir ), klorofil molekülleri (yeşil noktalar) molekülleri ışık enerjisini absorbe ederek merkezdeki P680 molekülüne (kırmızı renkli) kadar iletirler ), klorofil molekülleri (yeşil noktalar) molekülleri ışık enerjisini absorbe ederek merkezdeki P680 molekülüne (kırmızı renkli) kadar iletirler P680, suyun parçalanması ile serbest kalan 2 elektronu, henüz keşfedilememiş bir aracı moleküle iletir P680, suyun parçalanması ile serbest kalan 2 elektronu, henüz keşfedilememiş bir aracı moleküle iletir Elektronlar bu molekül üzerinden " Plastokinon (PQH) " ' a gelir  Plastokinon kendini redükte etmek için stromadan yani tilakoid membranının dış tarafından yada diğer bir deyimiyle kloroplastın iç tarafından H (+) iyonunu alır Plastokinon kendini redükte etmek için stromadan yani tilakoid membranının dış tarafından yada diğer bir deyimiyle kloroplastın iç tarafından H (+) iyonunu alır Elektronlar plastokinondan çıktıktan sonra Sitokrom - f ' ye giderken ATP senezine katılır Elektronlar plastokinondan çıktıktan sonra Sitokrom - f ' ye giderken ATP senezine katılır Sitokfom - f ye gelen elektron ardından merkezinde P700 molekülü bulunan diğer kuantozoma gelir (Bu kuantozomda fotosistem 1 dir) Sitokfom - f ye gelen elektron ardından merkezinde P700 molekülü bulunan diğer kuantozoma gelir (Bu kuantozomda fotosistem 1 dir) Fotosistem 1 e ulaşan elektronlar buradan, yapısında demir ve sülfür bulunduran protein kompleksine gelir Fotosistem 1 e ulaşan elektronlar buradan, yapısında demir ve sülfür bulunduran protein kompleksine gelir Elektronların buradan sonra izleyebileceği iki yol vardır Elektronların buradan sonra izleyebileceği iki yol vardır Ya Sitokrom - b6 üzerinden plastokinona geri döner, yada ferredoksin molekülüne giderek NADPH sentezini gerçekleştirir  P680 molekülü P700 molekülüne göre daha kısa dalga boyuna sahip ışınları absorbe eder  Eğer P680 sistemi çalışmaz ise su parçalanamayacağı için H (+) iyonu serbest kalamayacak ve NADP redüklenemeyecektir Eğer P680 sistemi çalışmaz ise su parçalanamayacağı için H (+) iyonu serbest kalamayacak ve NADP redüklenemeyecektir Dolayısıyla P700 sistemi elektronunu demir sülfürlü protein üzerinden sitokrom - b6 ya fırlatarak bir döngü oluşmasını sağlar Dolayısıyla P700 sistemi elektronunu demir sülfürlü protein üzerinden sitokrom - b6 ya fırlatarak bir döngü oluşmasını sağlar İşte bu şekilde bir elektron döngüsüyle ATP sentezlenmesi olayına " Devresel İşte bu şekilde bir elektron döngüsüyle ATP sentezlenmesi olayına " Devreselfotofosforilasyon " denir  Eğer P680 sistemi aktif ise, suyun parçalanmasıyla serbest kalan 2 elektronu kazandığı gibi plastokinona ve oradanda P700 sistemine gönderir  P700 den fırlatılan elektronlar, demir sülfürlü protein üzerinden " Ferredoksin " ' e ulaşır ve ortamdaki serbest H (+) iyonlarını kullanılarak NADPH sentezini gerçekleştirilir P700 den fırlatılan elektronlar, demir sülfürlü protein üzerinden " Ferredoksin " ' e ulaşır ve ortamdaki serbest H (+) iyonlarını kullanılarak NADPH sentezini gerçekleştirilir P680 tarafından verilen elektronlar molekülün bulunduğu kuantozoma bir daha dönmediği için bu şekilde NADPH sentezlenmesi olayına P680 tarafından verilen elektronlar molekülün bulunduğu kuantozoma bir daha dönmediği için bu şekilde NADPH sentezlenmesi olayınaise " Devresel olmayan fotofosforilasyon " adı verilir  Stromadan plastokinon (PQH) ' a gelen hidrojen, yine plastokinon üzerinden lümene geçer  Plastokinon burada H (+) iyonunu ileten bir mekik görevi üstlenmiştir Plastokinon burada H (+) iyonunu ileten bir mekik görevi üstlenmiştir H (+) iyonları lümene geçtikten sonra aşağıdaki şekilde gösterildiği gibi ATP sentezlenir H (+) iyonları lümene geçtikten sonra aşağıdaki şekilde gösterildiği gibi ATP sentezlenir 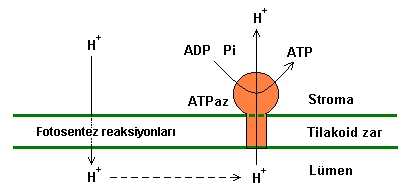 Bu mükemmel sistem sayesinde bitki kendi bünyesi için ATP üretip enerji sağlarken, aynı zamanda yaşamımız için gerekli olan oksijenide atmosfere serbest bırakmış olur  Doğada atmosfere serbest bırakılan oksijenin % 80 ' i deniz bitkileri ve fotosentez yapan mikroorganizmalar tarafından üretilir  Geriye kalan % 20 lik kısım ise kara bitkileri tarafından üretilir Geriye kalan % 20 lik kısım ise kara bitkileri tarafından üretilir Bitkiler ürettikleri ATP enerjisini kullanarak glikoz ve karbonhidrat moleküllerini sentezlemektedir Bitkiler ürettikleri ATP enerjisini kullanarak glikoz ve karbonhidrat moleküllerini sentezlemektedir Üretilen bu maddelerin yanlızca % 10 luk kısmı besin kaynağı olarak doğaya sunulurken, % 90 lık kısmını ise bitki, kendi yapısal organizasyonunu kurmak için kullanır Üretilen bu maddelerin yanlızca % 10 luk kısmı besin kaynağı olarak doğaya sunulurken, % 90 lık kısmını ise bitki, kendi yapısal organizasyonunu kurmak için kullanır Mesela gövdenin odunlaşması gibi Mesela gövdenin odunlaşması gibi Fotosentezin hızı ise çeşitli faktörlere bağlıdır  Bu faktörler arasında ortamın CO2 konsantrasyonu, sıcaklık, bitkinin topraktan çektiği su miktarı, nemlilik ve yaprak yapısı bu faktörlerin başında gelir Bu faktörler arasında ortamın CO2 konsantrasyonu, sıcaklık, bitkinin topraktan çektiği su miktarı, nemlilik ve yaprak yapısı bu faktörlerin başında gelir Fotosentezde yukarıda anlattığımız sisteme alternatif olarak değişik yollarda vardır  Bitkiler normalde gündüzleri yaprak stomalarını açarak CO2 yi absorbe eder ve aynı anda güneş ışığıyla birlikte fotosentez reaksiyonlarını gerçekleştirir Bitkiler normalde gündüzleri yaprak stomalarını açarak CO2 yi absorbe eder ve aynı anda güneş ışığıyla birlikte fotosentez reaksiyonlarını gerçekleştirir Fakat çöl bitkilerinde durum böyle değildir Fakat çöl bitkilerinde durum böyle değildir Çöllerde sıcaklık yüksek olduğu için bitki, stomalarını gündüz vakitlerinde kapalı tutar  Çünki açık tutması halinde bitki aşırı miktarda su kaybedecek ve ölecektir Çünki açık tutması halinde bitki aşırı miktarda su kaybedecek ve ölecektir Fakat stomalar açılmadan atmosferden CO2 absorbe etmekte mümkün değildir Fakat stomalar açılmadan atmosferden CO2 absorbe etmekte mümkün değildir Bitki bu problemin üstesinden nasıl gelmiştir ?  İnsanoğlu olarak kolay kolay çözüm bulamayacağımız bu büyük problemi, bitki kendisine verilen mükemmel enzimler sayesinde rahatlıkla çözmekte ve tıpkı diğer bitkiler gibi fotosentez yapıp ATP gereksinimini karşılamaktadır  Sistem şu şekilde çalışır ; 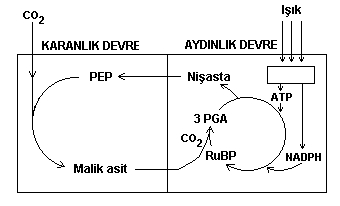 Yandaki şekilde bitkilerde CAM metabolizmasını anlatan çizim görülmektedir Yandaki şekilde bitkilerde CAM metabolizmasını anlatan çizim görülmektedir Bitkinin yaprakları gündüzleri kapalı olmasına karşın geceleri açıktır  Geceleri atmosferden absorbe ettiği CO2 gazını PEP (Fosfoenol pirüvik asit) ile reaksiyona sokarak " Malik asit " üretmektedir Geceleri atmosferden absorbe ettiği CO2 gazını PEP (Fosfoenol pirüvik asit) ile reaksiyona sokarak " Malik asit " üretmektedir Ürettiği malik asidi hücrelerindeki vakuollerde biriktirip depo eder Ürettiği malik asidi hücrelerindeki vakuollerde biriktirip depo eder Gündüzleri ise stomaları kapar ve bu nedenle artık hücrelere CO2 girişi durur  Fakat bitki CO2 gazını malik asiti parçalayarak elde eder Fakat bitki CO2 gazını malik asiti parçalayarak elde eder NADP, malik asiti dekarboksile eder ve NADPH ' a dönüşür NADP, malik asiti dekarboksile eder ve NADPH ' a dönüşür Malik asit dekarboksile olurken hem yapısındaki CO2 yi serbest bırakır hemde pirüvik asite dönüşür Malik asit dekarboksile olurken hem yapısındaki CO2 yi serbest bırakır hemde pirüvik asite dönüşür Pirüvik asit (3 karbonlu) daha sonra kalvin çemberi adı verilen reaksiyon basamakları ile 6 karbonlu şekerlere dönüştürülerek, geceleri tekrar PEP i vermek için reaksiyonlara katılır  Özet olarak ; Bitki geceleri absorbe ettiği karbondioksiti PEP yardımıyla malik asite çevirmekte, gündüzleri ise stomalarını kapayarak malik asiti parçalayıp karbondioksit gazını tekrar elde etmektedir  Bitkinin bu şekilde asit sentezleyip bu asiti gerektiği zaman yıkması olayına " Crassulacean asit metabolizması (CAM) " adı verilir Bitkinin bu şekilde asit sentezleyip bu asiti gerektiği zaman yıkması olayına " Crassulacean asit metabolizması (CAM) " adı verilir Buraya kadar anlatılan kimyasal reaksiyonlar bitki ve hayvan organizmalarındaki karmaşayı gözler önüne sermektedir  Hücrenin kendi içerisinde bile olağan üstü karmaşa içerisinde metabolik olaylar cereyan etmektdir Hücrenin kendi içerisinde bile olağan üstü karmaşa içerisinde metabolik olaylar cereyan etmektdir Milyarlarca trilyonlarca hücrenin birbirleriyle anlaşarak eşi benzeri olmayan kimyasal fabrikalar gibi çalışması, canlıların yapısal organizasyonlarının kusursuz bir şekilde tasarlandığını ortaya koymaktadır Milyarlarca trilyonlarca hücrenin birbirleriyle anlaşarak eşi benzeri olmayan kimyasal fabrikalar gibi çalışması, canlıların yapısal organizasyonlarının kusursuz bir şekilde tasarlandığını ortaya koymaktadır Bugün teknolojisi, canlıların içerisinde yürüyen metabolik faaliyetlerin bir benzerini değil yapmak yanından bile geçememektedir  Buraya kadar anlatmaya çalıştığımız onlarca metabolik faaliyetler, hücre içinde yürüyen kimyasal reaksiyonların yanında çöldeki kum tanesi kadar kalmaktadır Buraya kadar anlatmaya çalıştığımız onlarca metabolik faaliyetler, hücre içinde yürüyen kimyasal reaksiyonların yanında çöldeki kum tanesi kadar kalmaktadır |

|
Üye olmanıza kesinlikle gerek yok !
Konuya yorum yazmak için sadece buraya tıklayınız.
Bu sitede 1 günde 10.000 kişiye sesinizi duyurma fırsatınız var.
IP adresleri kayıt altında tutulmaktadır. Aşağılama, hakaret, küfür vb. kötü içerikli mesaj yazan şahıslar IP adreslerinden tespit edilerek haklarında suç duyurusunda bulunulabilir.
Konuya yorum yazmak için sadece buraya tıklayınız.
Bu sitede 1 günde 10.000 kişiye sesinizi duyurma fırsatınız var.
IP adresleri kayıt altında tutulmaktadır. Aşağılama, hakaret, küfür vb. kötü içerikli mesaj yazan şahıslar IP adreslerinden tespit edilerek haklarında suç duyurusunda bulunulabilir.
«
Önceki Konu
|
Sonraki Konu
»
| Konu Araçları | Bu Konuda Ara |
| Görünüm Modları | |
|
|
ForumSinsi.com hakkında yapılacak tüm şikayetlerde ilgili adresimizle iletişime geçilmesi halinde kanunlar ve yönetmelikler çerçevesinde en geç 1 (Bir) Hafta içerisinde gereken işlemler yapılacaktır. İletişime geçmek için buraya tıklayınız.





